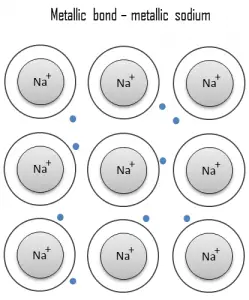
Une liaison métallique est une liaison chimique, dans laquelle les atomes ne partagent pas ou n’échangent pas d’électrons pour se lier. Au lieu de cela, de nombreux électrons (environ un pour chaque atome) sont plus ou moins libres de se déplacer dans le métal, de sorte que chaque électron peut interagir avec de nombreux atomes fixes. Les électrons libres protègent les noyaux ioniques chargés positivement des forces électrostatiques mutuellement répulsives qu’ils exerceraient autrement les uns sur les autres; par conséquent, la liaison métallique est de caractère non directionnel. La liaison métallique se trouve dans les métaux et leurs alliages. Le libre mouvement ou la délocalisation des électrons de liaison conduit à des propriétés métalliques classiques telles que le lustre (réflectivité de la lumière de surface), la conductivité électrique et thermique, la ductilité et la résistance à la traction élevée. La métallurgie est un domaine de la science des matériaux et de l’ingénierie des matériaux qui étudie le comportement physique et chimique des éléments métalliques et de leurs alliages. La métallurgie concerne les propriétés et structures chimiques, physiques et atomiques des métaux et les principes selon lesquels les métaux sont combinés pour former des alliages. La métallurgie est utilisée pour séparer les métaux de leur minerai. La métallurgie se subdivise en métallurgie ferreuse (métallurgie du fer et de ses alliages également appelée métallurgie noire) et métallurgie non ferreuse (métallurgie de l’aluminium, du cuivre, etc.). La métallurgie ferreuse implique des procédés et des alliages à base de fer tandis que la métallurgie non ferreuse implique des procédés et des alliages à base d’autres métaux. Un alliage est un mélange de deux matériaux ou plus, dont au moins un est un métal. Les alliages peuvent avoir une microstructure consistant en des solutions solides, où des atomes secondaires sont introduits comme substituts ou interstitiels dans un réseau cristallin. Un alliage peut également être un mélange de phases métalliques (deux solutions ou plus, formant une microstructure de cristaux différents au sein du métal). Des exemples d’alliages de substitution comprennent le bronze et le laiton, dans lesquels certains des atomes de cuivre sont respectivement remplacés par des atomes d’étain ou de zinc. Les solutions solides ont d’importantes applications commerciales et industrielles, car ces mélanges ont souvent des propriétés supérieures aux matériaux purs. De nombreux alliages métalliques sont des solutions solides. Même de petites quantités de soluté peuvent affecter les propriétés électriques et physiques du solvant. L’alliage est une pratique courante car les liaisons métalliques permettent l’assemblage de différents types de métaux. Par exemple, les aciers inoxydables austénitiques, y compris l’acier inoxydable de type 304 (contenant 18 % à 20 % de chrome et 8 % à 10,5 % de nickel), ont une structure cubique face centrée d’atomes de fer avec le carbone en solution solide interstitielle. Les alliages ferreux, ceux dont le fer est le principal constituant, comprennent l’acier et la fonte brute (avec une teneur en carbone de quelques pour cent) et les alliages de fer avec d’autres métaux (comme l’acier inoxydable). Les alliages ferreux sont connus pour leur résistance. Les alliages sont généralement plus résistants que les métaux purs, bien qu’ils offrent généralement une conductivité électrique et thermique réduite. Les alliages ferreux les plus simples sont connus sous le nom d’aciers et ils sont constitués de fer (Fe) allié au carbone (C) (environ 0,1% à 1%, selon le type). L’ajout d’une petite quantité de carbone non métallique au fer échange sa grande ductilité contre une plus grande résistance. En raison de sa très haute résistance, mais toujours de sa ténacité substantielle, et de sa capacité à être fortement altérée par le traitement thermique, l’acier est l’un des alliages ferreux les plus utiles et les plus courants dans l’utilisation moderne. Voir aussi: Qu’est-ce qu’une solution solide ? Historiquement, la transformation des métaux est l’un des domaines clés de la science des matériaux. La science des matériaux est l’une des plus anciennes formes d’ingénierie et de science appliquée et le matériau de choix d’une époque donnée est souvent un point déterminant (par exemple l’âge de pierre, l’âge du bronze, l’âge du fer). La transformation des métaux comprend la production d’ alliages, la mise en forme, le traitement thermique et le traitement de surface du produit. La détermination de la dureté du métal à l’aide des échelles de dureté Rockwell, Vickers et Brinell est une pratique couramment utilisée qui permet de mieux comprendre l’élasticité et la plasticité du métal pour différentes applications et processus de production. La tâche des ingénieurs matériaux est d’atteindre un équilibre entre les propriétés des matériaux telles que le coût, le poids, la résistance, la ténacité, la dureté, la corrosion, la résistance à la fatigue et les performances à des températures extrêmes. Pour atteindre cet objectif, l’environnement d’exploitation doit être soigneusement étudié. Dans un environnement d’eau salée, les métaux ferreux et certains alliages d’aluminium se corrodent rapidement. Les métaux exposés à des conditions froides ou cryogéniques peuvent subir une transition ductile à fragile et perdent leur ténacité, devenant plus fragiles et susceptibles de se fissurer. Les métaux soumis à une charge cyclique continue peuvent souffrir de fatigue du métal. Les métaux soumis à des contraintes constantes à des températures élevées peuvent fluer.
La transformation des métaux à l’état solide peut être divisée en deux grandes étapes: Traitement thermique des métaux Les métaux peuvent être traités thermiquement pour modifier les propriétés de résistance, de ductilité, de ténacité, de dureté ou de résistance à la corrosion. Il existe un certain nombre de phénomènes qui se produisent dans les métaux et alliages à des températures élevées. Par exemple, la recristallisation et la décomposition de l’austénite. Ceux-ci sont efficaces pour modifier les caractéristiques mécaniques lorsque des traitements thermiques ou des processus thermiques appropriés sont utilisés. En fait, l’utilisation de traitements thermiques sur les alliages commerciaux est une pratique extrêmement courante. Les processus de traitement thermique courants comprennent le recuit, le durcissement par précipitation, la trempe et le revenu. Le métal est un matériau (généralement solide) comprenant un ou plusieurs éléments métalliques (par exemple, le fer, l’aluminium, le cuivre, le chrome, le titane, l’or, le nickel), et souvent aussi des éléments non métalliques (par exemple, le carbone, l’azote, l’oxygène) en quantités relativement faibles.. La particularité des métaux en ce qui concerne leur structure est la présence de porteurs de charge, en particulier d’ électrons. Cette caractéristique est donnée par la nature de la liaison métallique. Les conductivités électrique et thermique des métaux proviennent du fait que leurles électrons externes sont délocalisés.
Le métal est un matériau (généralement solide) comprenant un ou plusieurs éléments métalliques (par exemple, le fer, l’aluminium, le cuivre, le chrome, le titane, l’or, le nickel), et souvent aussi des éléments non métalliques (par exemple, le carbone, l’azote, l’oxygène) en quantités relativement faibles.. La particularité des métaux en ce qui concerne leur structure est la présence de porteurs de charge, en particulier d’ électrons. Cette caractéristique est donnée par la nature de la liaison métallique. Les conductivités électrique et thermique des métaux proviennent du fait que leurles électrons externes sont délocalisés.Lien métallique
Métallurgie

Alliages
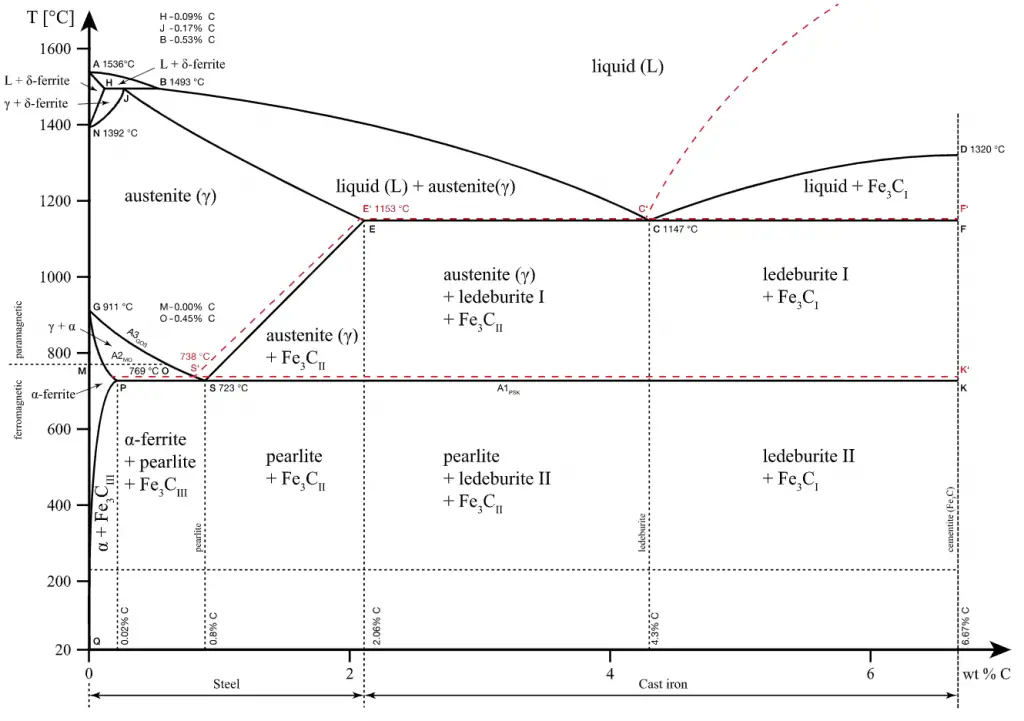
Traitement des métaux
Processus de travail des métaux
Processus d’assemblage
Traitement divers des métaux
Département américain de l’énergie, science des matériaux. DOE Fundamentals Handbook, Volume 1 and 2. Janvier 1993.
US Department of Energy, Material Science. DOE Fundamentals Handbook, Volume 2 et 2. Janvier 1993.
William D. Callister, David G. Rethwisch. Science et génie des matériaux : une introduction 9e édition, Wiley ; 9 édition (4 décembre 2013), ISBN-13 : 978-1118324578.
En ligneEberhart, Mark (2003). Pourquoi les choses se cassent : Comprendre le monde par la manière dont il se décompose. Harmonie. ISBN 978-1-4000-4760-4.
Gaskell, David R. (1995). Introduction à la thermodynamique des matériaux (4e éd.). Éditions Taylor et Francis. ISBN 978-1-56032-992-3.
González-Viñas, W. & Mancini, HL (2004). Une introduction à la science des matériaux. Presse universitaire de Princeton. ISBN 978-0-691-07097-1.
Ashby, Michael; Hugh Shercliff; David Cebon (2007). Matériaux: ingénierie, science, traitement et conception (1ère éd.). Butterworth-Heinemann. ISBN 978-0-7506-8391-3.
JR Lamarsh, AJ Baratta, Introduction au génie nucléaire, 3e éd., Prentice-Hall, 2001, ISBN : 0-201-82498-1.
Nous espérons que cet article, Métaux – Que sont les métaux, vous aidera. Si oui, donnez-nous un like dans la barre latérale. L’objectif principal de ce site Web est d’aider le public à apprendre des informations intéressantes et importantes sur les matériaux et leurs propriétés.