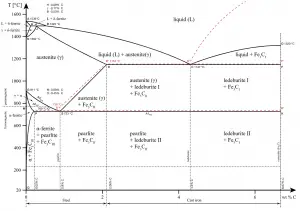
La cémentite (Fe3C) est un composé métastable et, dans certaines circonstances, elle peut être amenée à se dissocier ou à se décomposer pour former de la ferrite α et du graphite, selon la réaction :
Fe3C → 3Fe (α) + C (graphite)
Le temps de décomposition est long et il prendra beaucoup plus de temps que la durée de vie de l’application à température ambiante. D’autres facteurs (températures élevées et ajout de certains éléments d’alliage par exemple) peuvent affecter cette décomposition car ils favorisent la formation de graphite.
La cémentite dans sa forme pure est une céramique et elle est dure et cassante, ce qui la rend appropriée pour le renforcement des aciers. Ses propriétés mécaniques sont fonction de sa microstructure, qui dépend de la manière dont il est mélangé à la ferrite.
Dans le système fer-carbone (c’est-à-dire les aciers au carbone ordinaire et les fontes), il s’agit d’un constituant courant car la ferrite peut contenir au plus 0,02 % en poids de carbone non combiné. Ainsi, dans les aciers au carbone et les fontes à refroidissement lent, une partie du carbone se présente sous forme de cémentite.
La cémentite se forme directement à partir de la fonte dans le cas de la fonte blanche. Avec une teneur en silicium plus faible (contenant moins de 1,0 % en poids de Si – agent de graphitisation) et une vitesse de refroidissement plus rapide, le carbone de la fonte précipite hors de la fonte sous forme de cémentite en phase métastable, Fe3C, plutôt que de graphite. Le produit de cette solidification est connu sous le nom de fonte blanche (également appelée fonte refroidie).
Dans l’acier au carbone, la cémentite précipite à partir de l’austénite lorsque l’austénite se transforme en ferrite lors d’un refroidissement lent ou en martensite lors de la trempe. Un mélange intime avec la ferrite, l’autre produit de l’austénite, forme une structure lamellaire appelée perlite.
Dans les fontes, la formation de graphite est favorisée par la présence de silicium à des concentrations supérieures à environ 1 % en poids. De plus, des vitesses de refroidissement plus lentes pendant la solidification favorisent la graphitisation (la formation de graphite).
Autres phases courantes dans les aciers et les fers
Le traitement thermique des aciers nécessite une compréhension à la fois des phases d’équilibre et des phases métastables qui se produisent lors du chauffage et/ou du refroidissement. Pour les aciers, les phases d’équilibre stable comprennent :
- Ferrite. La ferrite ou α-ferrite est une phase de structure cubique centrée du fer qui existe en dessous de températures de 912 °C pour de faibles concentrations de carbone dans le fer. L’α-ferrite ne peut dissoudre que jusqu’à 0,02 % de carbone à 727 °C. Cela est dû à la configuration du réseau de fer qui forme une structure cristalline BCC. La phase primaire de l’acier à faible teneur en carbone ou doux et de la plupart des fontes à température ambiante est ferromagnétique α-Fe.
- Austénite. L’austénite, également connue sous le nom de fer en phase gamma (γ-Fe), est une phase de fer à structure cubique à faces centrées non magnétique. L’austénite dans les alliages fer-carbone n’est généralement présente qu’au-dessus de la température eutectoïde critique (723 °C) et en dessous de 1500 °C, selon la teneur en carbone. Cependant, il peut être conservé à température ambiante par des ajouts d’alliages tels que le nickel ou le manganèse. Le carbone joue un rôle important dans le traitement thermique, car il élargit la plage de température de stabilité de l’austénite. Une teneur en carbone plus élevée abaisse la température nécessaire pour austénitiser l’acier, de sorte que les atomes de fer se réarrangent pour former une structure de réseau fcc. L’austénite est présente dans le type d’acier inoxydable le plus couramment utilisé, qui est très connu pour sa résistance à la corrosion.
- Graphite. L’ajout d’une petite quantité de carbone non métallique au fer échange sa grande ductilité contre une plus grande résistance.
- Cémentite. La cémentite (Fe3C) est un composé métastable et, dans certaines circonstances, on peut la dissocier ou la décomposer pour former de l’α-ferrite et du graphite, selon la réaction: Fe3C → 3Fe (α) + C (graphite). La cémentite dans sa forme pure est une céramique et elle est dure et cassante, ce qui la rend appropriée pour le renforcement des aciers. Ses propriétés mécaniques sont fonction de sa microstructure, qui dépend de la manière dont il est mélangé à la ferrite.
Les phases métastables sont:
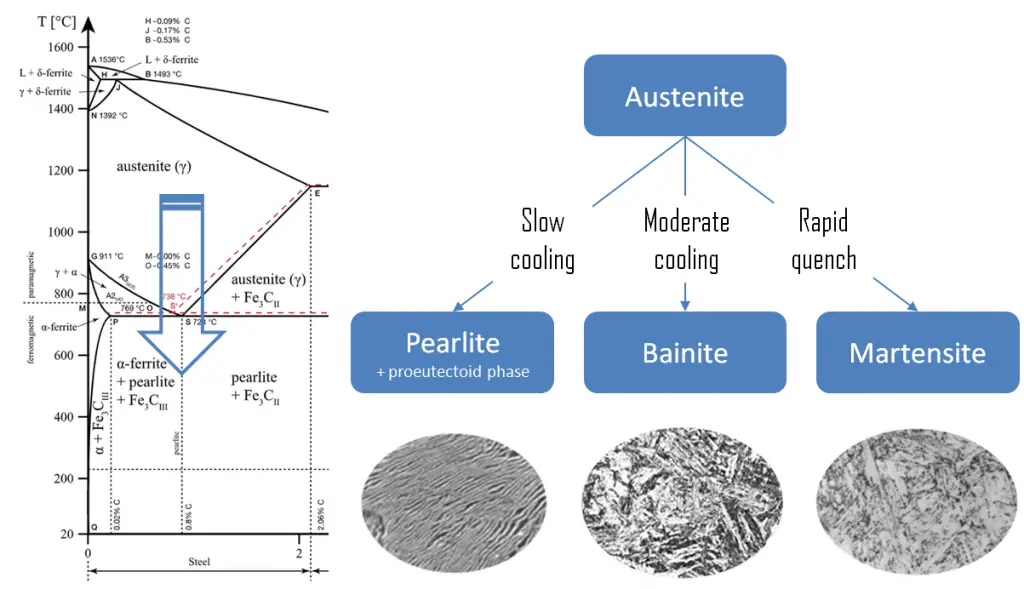 Perlite. En métallurgie, la perlite est une structure métallique en couches de deux phases, qui se compose de couches alternées de ferrite (87,5 % en poids) et de cémentite (12,5 % en poids) que l’on trouve dans certains aciers et fontes. Il est nommé pour sa ressemblance avec la nacre.
Perlite. En métallurgie, la perlite est une structure métallique en couches de deux phases, qui se compose de couches alternées de ferrite (87,5 % en poids) et de cémentite (12,5 % en poids) que l’on trouve dans certains aciers et fontes. Il est nommé pour sa ressemblance avec la nacre.- Martensite. La martensite est une structure métastable très dure avec une structure cristalline tétragonale centrée sur le corps (BCT). La martensite se forme dans les aciers lorsque la vitesse de refroidissement de l’austénite est si élevée que les atomes de carbone n’ont pas le temps de se diffuser hors de la structure cristalline en quantité suffisante pour former de la cémentite (Fe3C).
- Baïnite. La bainite est une microstructure en forme de plaque qui se forme dans les aciers à partir d’austénite lorsque les vitesses de refroidissement ne sont pas
assez rapides pour produire de la martensite mais sont encore assez rapides pour que le carbone n’ait pas assez de temps pour se diffuser pour former de la perlite. Les aciers bainitiques sont généralement plus résistants et plus durs que les aciers perlitiques; pourtant, ils présentent une combinaison souhaitable de résistance et de ductilité.
Département américain de l’énergie, science des matériaux. DOE Fundamentals Handbook, Volume 1 and 2. Janvier 1993.
US Department of Energy, Material Science. DOE Fundamentals Handbook, Volume 2 et 2. Janvier 1993.
William D. Callister, David G. Rethwisch. Science et génie des matériaux : une introduction 9e édition, Wiley ; 9 édition (4 décembre 2013), ISBN-13 : 978-1118324578.
En ligneEberhart, Mark (2003). Pourquoi les choses se cassent : Comprendre le monde par la manière dont il se décompose. Harmonie. ISBN 978-1-4000-4760-4.
Gaskell, David R. (1995). Introduction à la thermodynamique des matériaux (4e éd.). Éditions Taylor et Francis. ISBN 978-1-56032-992-3.
González-Viñas, W. & Mancini, HL (2004). Une introduction à la science des matériaux. Presse universitaire de Princeton. ISBN 978-0-691-07097-1.
Ashby, Michael; Hugh Shercliff; David Cebon (2007). Matériaux: ingénierie, science, traitement et conception (1ère éd.). Butterworth-Heinemann. ISBN 978-0-7506-8391-3.
JR Lamarsh, AJ Baratta, Introduction au génie nucléaire, 3e éd., Prentice-Hall, 2001, ISBN : 0-201-82498-1.
Nous espérons que cet article, Cementite – Fe3C, vous aidera. Si oui, donnez-nous un like dans la barre latérale. L’objectif principal de ce site Web est d’aider le public à apprendre des informations intéressantes et importantes sur les matériaux et leurs propriétés.