Une solution solide est un mélange uniforme de deux solides cristallins qui partagent un réseau cristallin commun. Les solutions solides sont souvent constituées de deux ou plusieurs types d’atomes ou de molécules qui partagent un réseau cristallin, comme dans certains alliages métalliques. Le solvant est l’élément ou le composé qui est présent en plus grande quantité. Soluté est utilisé pour désigner un élément ou un composé présent à une concentration mineure. Le soluté peut s’incorporer dans le réseau cristallin de solvant par substitution, en remplaçant une particule de solvant dans le réseau, ou de manière interstitielle, en s’insérant dans l’espace entre les particules de solvant. Ces deux types de solution solide affectent les propriétés du matériau en déformant le réseau cristallin et en perturbant l’homogénéité physique et électrique du matériau solvant.
Pour le type substitutionnel, les atomes de soluté ou d’impureté remplacent ou se substituent aux atomes hôtes. Plusieurs caractéristiques des atomes de soluté et de solvant déterminent le degré auquel le premier se dissout dans le second. Celles-ci sont exprimées par les règles de Hume-Rothery. Selon ces règles, des solutions solides de substitution peuvent se former si le soluté et le solvant ont:
- Rayons atomiques similaires (différence de 15 % ou moins)
- Même structure cristalline
- Électronégativités similaires
- De valence similaire, une solution solide se mélange avec d’autres pour former une nouvelle solution
Les solutions solides ont d’importantes applications commerciales et industrielles, car ces mélanges ont souvent des propriétés supérieures aux matériaux purs. De nombreux alliages métalliques sont des solutions solides. Même de petites quantités de soluté peuvent affecter les propriétés électriques et physiques du solvant.
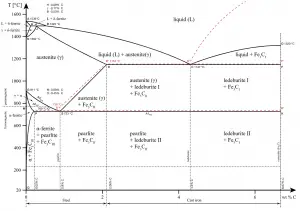
L’alliage est une pratique courante car les liaisons métalliques permettent l’assemblage de différents types de métaux. Par exemple, les aciers inoxydables austénitiques, y compris l’acier inoxydable de type 304 (contenant 18 % à 20 % de chrome et 8 % à 10,5 % de nickel), ont une structure cubique face centrée d’atomes de fer avec le carbone en solution solide interstitielle.
- Département américain de l’énergie, science des matériaux. DOE Fundamentals Handbook, Volume 1 et 2. Janvier 1993.
- Département américain de l’énergie, science des matériaux. DOE Fundamentals Handbook, Volume 2 et 2. Janvier 1993.
- William D. Callister, David G. Rethwisch. Science et génie des matériaux : une introduction 9e édition, Wiley ; 9 édition (4 décembre 2013), ISBN-13 : 978-1118324578.
- En ligneEberhart, Mark (2003). Pourquoi les choses se cassent : Comprendre le monde par la manière dont il se décompose. Harmonie. ISBN 978-1-4000-4760-4.
- Gaskell, David R. (1995). Introduction à la thermodynamique des matériaux (4e éd.). Éditions Taylor et Francis. ISBN 978-1-56032-992-3.
- Gonzalez-Viñas, W. & Mancini, HL (2004). Une introduction à la science des matériaux. Presse universitaire de Princeton. ISBN 978-0-691-07097-1
- Ashby, Michael; Hugh Shercliff; David Cebon (2007). Matériaux: ingénierie, science, traitement et conception (1ère éd.). Butterworth-Heinemann. ISBN 978-0-7506-8391-3.
- JR Lamarsh, AJ Baratta, Introduction au génie nucléaire, 3e éd., Prentice-Hall, 2001, ISBN : 0-201-82498-1.
Nous espérons que cet article, Solution solide – Matériaux, vous aidera. Si oui, donnez-nous un like dans la barre latérale. L’objectif principal de ce site Web est d’aider le public à apprendre des informations intéressantes et importantes sur les matériaux et leurs propriétés.