Liaisons intermoléculaires
Les forces intermoléculaires sont les forces qui médient l’interaction entre les molécules, y compris les forces d’attraction ou de répulsion qui agissent entre les molécules et d’autres types de particules voisines. Les forces intermoléculaires attractives et leurs liaisons résultantes sont classées dans les types suivants:
- Liaison moléculaire. Lorsque les électrons des atomes neutres passent plus de temps dans une région de leur orbite, une faible charge temporaire existera. La molécule attirera faiblement d’autres molécules. Ceci est parfois appelé van der Waals ou liaisons moléculaires.
- Liaison hydrogène. Une liaison hydrogène peut être intermoléculaire (se produisant entre des molécules distinctes) ou intramoléculaire (se produisant entre des parties de la même molécule). La liaison hydrogène est une force d’attraction principalement électrostatique entre un atome d’hydrogène (H) qui est lié de manière covalente à un atome ou un groupe plus électronégatif.
Liaison hydrogène
 Une liaison hydrogène peut être intermoléculaire (se produisant entre des molécules distinctes) ou intramoléculaire (se produisant entre des parties de la même molécule). La liaison hydrogène est une force d’attraction principalement électrostatique entre un atome d’hydrogène (H) qui est lié de manière covalente à un atome ou un groupe plus électronégatif.
Une liaison hydrogène peut être intermoléculaire (se produisant entre des molécules distinctes) ou intramoléculaire (se produisant entre des parties de la même molécule). La liaison hydrogène est une force d’attraction principalement électrostatique entre un atome d’hydrogène (H) qui est lié de manière covalente à un atome ou un groupe plus électronégatif.
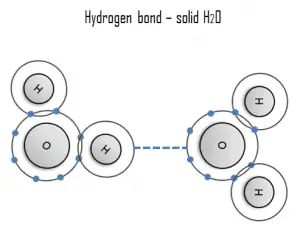
Un hydrogène est un exemple fort d’interaction entre deux dipôles permanents. La grande différence d’électronégativité entre l’hydrogène et le fluor, l’azote et l’oxygène, couplée à leurs paires d’électrons isolés, provoque de fortes forces électrostatiques entre les molécules. Un exemple omniprésent de liaison hydrogène se trouve entre les molécules d’eau. Les liaisons hydrogène sont responsables des points d’ébullition élevés de l’eau. Chaque molécule H2O a deux atomes d’hydrogène qui peuvent se lier à des atomes d’oxygène. De plus, son seul atome O peut se lier à deux atomes d’hydrogène d’autres H2O molécules. Ainsi, pour la glace solide, chaque molécule d’eau participe à quatre liaisons hydrogène, contribuant à créer un réseau hexagonal ouvert. Le point d’ébullition élevé de l’eau liquide est dû au nombre élevé de liaisons hydrogène que chaque molécule peut former, par rapport à sa faible masse moléculaire. En raison de la difficulté de rompre ces liaisons, l’eau a un point d’ébullition, un point de fusion et une viscosité très élevés par rapport à des liquides par ailleurs similaires non reliés par des liaisons hydrogène.
- Département américain de l’énergie, science des matériaux. DOE Fundamentals Handbook, Volume 1 et 2. Janvier 1993.
- Département américain de l’énergie, science des matériaux. DOE Fundamentals Handbook, Volume 2 et 2. Janvier 1993.
- William D. Callister, David G. Rethwisch. Science et génie des matériaux : une introduction 9e édition, Wiley ; 9 édition (4 décembre 2013), ISBN-13 : 978-1118324578.
- En ligneEberhart, Mark (2003). Pourquoi les choses se cassent : Comprendre le monde par la manière dont il se décompose. Harmonie. ISBN 978-1-4000-4760-4.
- Gaskell, David R. (1995). Introduction à la thermodynamique des matériaux (4e éd.). Éditions Taylor et Francis. ISBN 978-1-56032-992-3.
- Gonzalez-Viñas, W. & Mancini, HL (2004). Une introduction à la science des matériaux. Presse universitaire de Princeton. ISBN 978-0-691-07097-1
- Ashby, Michael; Hugh Shercliff; David Cebon (2007). Matériaux: ingénierie, science, traitement et conception (1ère éd.). Butterworth-Heinemann. ISBN 978-0-7506-8391-3.
- JR Lamarsh, AJ Baratta, Introduction au génie nucléaire, 3e éd., Prentice-Hall, 2001, ISBN : 0-201-82498-1.
Nous espérons que cet article, Liens intermoléculaires, vous aidera. Si oui, donnez-nous un like dans la barre latérale. L’objectif principal de ce site Web est d’aider le public à apprendre des informations intéressantes et importantes sur les matériaux et leurs propriétés.