Les propriétés thermiques des matériaux font référence à la réponse des matériaux aux changements de leur thermodynamics/thermodynamic-properties/what-is-temperature-physics/ »>température et à l’application de chaleur. Lorsqu’un solide absorbe de thermodynamics/what-is-energy-physics/ »>l’énergie sous forme de chaleur, sa température augmente et ses dimensions augmentent. Mais différents matériaux réagissent différemment à l’application de chaleur.
La capacité calorifique, la dilatation thermique et la conductivité thermique sont des propriétés qui sont souvent critiques dans l’utilisation pratique des solides.
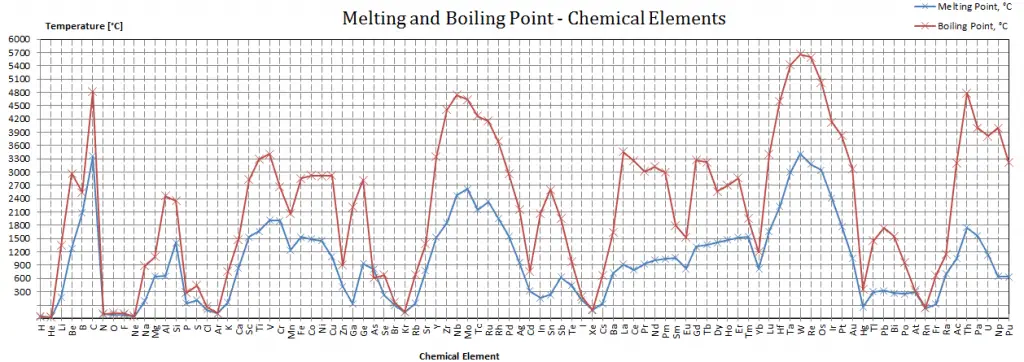
Point d’ébullition des matériaux
Notez que ces points sont associés à la pression atmosphérique standard.
Voir aussi: Points d’ébullition – Tableau périodique
En général, l’ébullition est un changement de phase d’une substance de la phase liquide à la phase gazeuse. Le point d’ébullition d’une substance est la température à laquelle se produit ce changement de phase (ébullition ou vaporisation). La température à laquelle la vaporisation (ébullition) commence à se produire pour une pression donnée est également connue sous le nom de température de saturation et dans ces conditions, un mélange de vapeur et de liquide peut exister ensemble. On peut dire que le liquide est saturé d’énergie thermique. Tout ajout d’énergie thermique entraîne une transition de phase. Au point d’ébullition les deux phases d’une substance, liquide et vapeur, ont des énergies libres identiques et sont donc également susceptibles d’exister. En dessous du point d’ébullition, le liquide est l’état le plus stable des deux, alors qu’au-dessus, la forme gazeuse est préférée. La pression à laquelle la vaporisation (ébullition) commence à se produire pour une température donnée est appelée la pression de saturation. Considérée comme la température du passage inverse de la vapeur au liquide, elle est appelée point de condensation.
Comme on peut le voir, le point d’ébullition d’un liquide varie en fonction de la pression environnementale environnante. Un liquide sous vide partiel a un point d’ébullition plus bas que lorsque ce liquide est à la pression atmosphérique. Un liquide à haute pression a un point d’ébullition plus élevé que lorsque ce liquide est à la pression atmosphérique. Par exemple, l’eau bout à 100 °C (212 °F) au niveau de la mer, mais à 93,4 °C (200,1 °F) à 1900 mètres (6 233 pieds) d’altitude. D’autre part, l’eau bout à 350 °C (662 °F) à 16,5 MPa (pression typique des REP).
Dans le tableau périodique des éléments, l’élément dont le point d’ébullition est le plus bas est l’hélium. Les points d’ébullition du rhénium et du tungstène dépassent 5000 K à la pression standard. Puisqu’il est difficile de mesurer précisément les températures extrêmes sans biais, les deux ont été cités dans la littérature comme ayant le point d’ébullition le plus élevé.
- Département américain de l’énergie, science des matériaux. DOE Fundamentals Handbook, Volume 1 et 2. Janvier 1993.
- Département américain de l’énergie, science des matériaux. DOE Fundamentals Handbook, Volume 2 et 2. Janvier 1993.
- William D. Callister, David G. Rethwisch. Science et génie des matériaux : une introduction 9e édition, Wiley ; 9 édition (4 décembre 2013), ISBN-13 : 978-1118324578.
- En ligneEberhart, Mark (2003). Pourquoi les choses se cassent : Comprendre le monde par la manière dont il se décompose. Harmonie. ISBN 978-1-4000-4760-4.
- Gaskell, David R. (1995). Introduction à la thermodynamique des matériaux (4e éd.). Éditions Taylor et Francis. ISBN 978-1-56032-992-3.
- Gonzalez-Viñas, W. & Mancini, HL (2004). Une introduction à la science des matériaux. Presse universitaire de Princeton. ISBN 978-0-691-07097-1
- Ashby, Michael; Hugh Shercliff; David Cebon (2007). Matériaux: ingénierie, science, traitement et conception (1ère éd.). Butterworth-Heinemann. ISBN 978-0-7506-8391-3.
- JR Lamarsh, AJ Baratta, Introduction au génie nucléaire, 3e éd., Prentice-Hall, 2001, ISBN : 0-201-82498-1.
Nous espérons que cet article, Point d’ébullition des matériaux, vous aidera. Si oui, donnez-nous un like dans la barre latérale. L’objectif principal de ce site Web est d’aider le public à apprendre des informations intéressantes et importantes sur les matériaux et leurs propriétés.