Fortalecimento de Metais
A resistência de metais e ligas pode ser modificada através de várias combinações de trabalho a frio, ligas e tratamento térmico. Conforme discutido na seção anterior, a capacidade de um material cristalino se deformar plasticamente depende em grande parte da capacidade do deslocamento se mover dentro de um material. Portanto, impedir o movimento das discordâncias resultará no fortalecimento do material. Por exemplo, uma microestrutura com grãos mais finos normalmente resulta em maior resistência e tenacidade superior em comparação com a mesma liga com grãos fisicamente maiores. No caso do tamanho do grão, também pode haver compensação entre as características de resistência e fluência. Outros mecanismos de reforço são alcançados à custa de menor ductilidade e tenacidade. Existem muitos mecanismos de fortalecimento, que incluem:
- Reforço de Solução Sólida (liga)
- Endurecimento por Trabalho (Trabalho a Frio)
- endurecimento por precipitação
- Refinamento de Grãos
- Endurecimento da Transformação
Reforço de Sólidos Sólidos – Liga
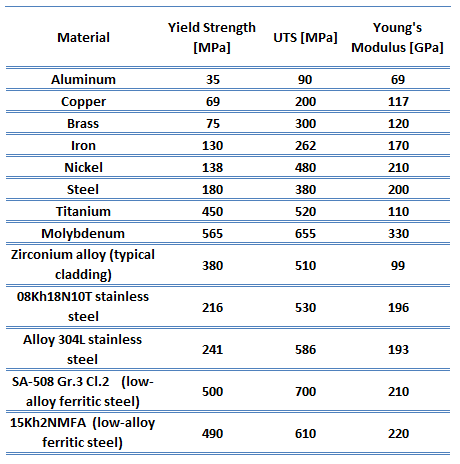 Átomos de diferentes elementos dissolvidos na fase matriz podem levar ao seu fortalecimento pelo fortalecimento da solução sólida. Os metais de alta pureza são quase sempre mais macios e fracos do que as ligas compostas do mesmo metal base. O aumento da concentração da impureza resulta em um aumento concomitante nas resistências à tração e ao escoamento. O soluto pode ser incorporado à rede cristalina do solvente de forma substitutiva, substituindo uma partícula de solvente na rede, ou intersticialmente, encaixando-se no espaço entre as partículas do solvente. Isso impõe tensões de rede nos átomos circundantes, resultando em um campo de tensão de rede. Mesmo pequenas quantidades de soluto podem afetar as propriedades elétricas e físicas do solvente. Aço, provavelmente o metal estrutural mais comum, é um bom exemplo de liga. É uma liga de ferro e carbono, com outros elementos que lhe conferem certas propriedades desejáveis. Adicionar uma pequena quantidade de carbono não metálico ao ferro troca sua grande ductilidade por maior resistência. Adicionar uma pequena quantidade de carbono não metálico ao ferro troca sua grande ductilidade por maior resistência. Para ligas não ferrosas, manganês e magnésio são exemplos de elementos adicionados ao alumínio com a finalidade de fortalecer a solução sólida.
Átomos de diferentes elementos dissolvidos na fase matriz podem levar ao seu fortalecimento pelo fortalecimento da solução sólida. Os metais de alta pureza são quase sempre mais macios e fracos do que as ligas compostas do mesmo metal base. O aumento da concentração da impureza resulta em um aumento concomitante nas resistências à tração e ao escoamento. O soluto pode ser incorporado à rede cristalina do solvente de forma substitutiva, substituindo uma partícula de solvente na rede, ou intersticialmente, encaixando-se no espaço entre as partículas do solvente. Isso impõe tensões de rede nos átomos circundantes, resultando em um campo de tensão de rede. Mesmo pequenas quantidades de soluto podem afetar as propriedades elétricas e físicas do solvente. Aço, provavelmente o metal estrutural mais comum, é um bom exemplo de liga. É uma liga de ferro e carbono, com outros elementos que lhe conferem certas propriedades desejáveis. Adicionar uma pequena quantidade de carbono não metálico ao ferro troca sua grande ductilidade por maior resistência. Adicionar uma pequena quantidade de carbono não metálico ao ferro troca sua grande ductilidade por maior resistência. Para ligas não ferrosas, manganês e magnésio são exemplos de elementos adicionados ao alumínio com a finalidade de fortalecer a solução sólida.
Agentes de Liga
O ferro puro é muito macio para ser usado como estrutura, mas a adição de pequenas quantidades de outros elementos (carbono, manganês ou silício, por exemplo) aumenta muito sua resistência mecânica. As ligas são geralmente mais fortes que os metais puros, embora geralmente ofereçam condutividade elétrica e térmica reduzida. A resistência é o critério mais importante pelo qual muitos materiais estruturais são julgados. Portanto, as ligas são usadas para construção de engenharia. O efeito sinérgico dos elementos de liga e do tratamento térmico produz uma enorme variedade de microestruturas e propriedades.
- Carbono. O carbono é um elemento não metálico, que é um importante elemento de liga em todos os materiais à base de metais ferrosos. O carbono está sempre presente nas ligas metálicas, ou seja, em todos os tipos de aço inoxidável e ligas resistentes ao calor. O carbono é um austenitizador muito forte e aumenta a resistência do aço. Na verdade, é o principal elemento de endurecimento e é essencial para a formação de cementita, Fe 3C, perlita, esferoidita e martensita ferro-carbono. Adicionar uma pequena quantidade de carbono não metálico ao ferro troca sua grande ductilidade por maior resistência. Se for combinado com cromo como constituinte separado (carboneto de cromo), pode ter um efeito prejudicial na resistência à corrosão, removendo parte do cromo da solução sólida na liga e, como consequência, reduzindo a quantidade de cromo disponível para garantir resistência à corrosão.
- Cromo. O cromo aumenta a dureza, força e resistência à corrosão. O efeito de fortalecimento da formação de carbonetos metálicos estáveis nos contornos de grão e o forte aumento na resistência à corrosão fizeram do cromo um importante material de liga para o aço. A resistência dessas ligas metálicas aos efeitos químicos de agentes corrosivos é baseada na passivação. Para que a passivação ocorra e permaneça estável, a liga Fe-Cr deve ter um teor mínimo de cromo de cerca de 11% em peso, acima do qual a passividade pode ocorrer e abaixo do qual é impossível. O cromo pode ser usado como um elemento de endurecimento e é freqüentemente usado com um elemento de endurecimento, como o níquel, para produzir propriedades mecânicas superiores. Em temperaturas mais altas, o cromo contribui com maior resistência. Os aços rápidos para ferramentas contêm entre 3 e 5% de cromo.
- Níquel. O níquel é um dos elementos de liga mais comuns. Cerca de 65% da produção de níquel é usada em aços inoxidáveis. Como o níquel não forma nenhum composto de carboneto no aço, ele permanece em solução na ferrita, fortalecendo e endurecendo a fase de ferrita. Aços de níquel são facilmente tratados termicamente porque o níquel reduz a taxa crítica de resfriamento. Ligas à base de níquel (por exemplo, ligas Fe-Cr-Ni(Mo)) exibem excelente ductilidade e tenacidade, mesmo em altos níveis de resistência e essas propriedades são mantidas até baixas temperaturas. O níquel também reduz a expansão térmica para melhor estabilidade dimensional. O níquel é o elemento base das superligas, que são um grupo de ligas de níquel, ferro-níquel e cobalto usadas em motores a jato. Esses metais têm excelente resistência à deformação por fluência térmica e mantêm sua rigidez, resistência,
- Molibdênio. Encontrado em pequenas quantidades em aços inoxidáveis, o molibdênio aumenta a temperabilidade e a resistência, principalmente em altas temperaturas. O alto ponto de fusão do molibdênio o torna importante para dar resistência ao aço e outras ligas metálicas em altas temperaturas. O molibdênio é único na medida em que aumenta a resistência à tração e à fluência do aço em altas temperaturas. Ele retarda a transformação de austenita em perlita muito mais do que a transformação de austenita em bainita; assim, a bainita pode ser produzida por resfriamento contínuo de aços contendo molibdênio.
- Vanádio. O vanádio é geralmente adicionado ao aço para inibir o crescimento do grão durante o tratamento térmico. Ao controlar o crescimento do grão, melhora a resistência e a tenacidade dos aços endurecidos e revenidos. O tamanho do grão determina as propriedades do metal. Por exemplo, tamanho de grão menor aumenta a resistência à tração e tende a aumentar a ductilidade. Um tamanho de grão maior é preferido para melhorar as propriedades de fluência em alta temperatura. O vanádio é adicionado para promover a resistência à abrasão e para produzir carbonetos duros e estáveis que, sendo apenas parcialmente solúveis, liberam pouco carbono na matriz.
- Tungstênio. Produz carbonetos estáveis e refina o tamanho do grão para aumentar a dureza, principalmente em altas temperaturas. O tungstênio é amplamente utilizado em aços para ferramentas de alta velocidade e foi proposto como substituto do molibdênio em aços ferríticos de ativação reduzida para aplicações nucleares. A adição de cerca de 10% de tungstênio e molibdênio no total maximiza com eficiência a dureza e a tenacidade dos aços rápidos e mantém essas propriedades nas altas temperaturas geradas no corte de metais. Tungstênio e molibdênio são intercambiáveis em nível atômico e ambos promovem resistência ao revenido, o que proporciona melhor desempenho de corte da ferramenta em temperaturas mais altas.
Departamento de Energia dos EUA, Ciência de Materiais. DOE Fundamentals Handbook, Volume 1 e 2. Janeiro de 1993.
Departamento de Energia dos EUA, Ciência de Materiais. DOE Fundamentals Handbook, Volume 2 e 2. Janeiro de 1993.
William D. Callister, David G. Rethwisch. Ciência e Engenharia de Materiais: Uma Introdução 9ª Edição, Wiley; 9 edição (4 de dezembro de 2013), ISBN-13: 978-1118324578.
Eberhart, Mark (2003). Por que as coisas quebram: entendendo o mundo pela maneira como ele se desfaz. Harmonia. ISBN 978-1-4000-4760-4.
Gaskell, David R. (1995). Introdução à Termodinâmica dos Materiais (4ª ed.). Editora Taylor e Francis. ISBN 978-1-56032-992-3.
González-Viñas, W. & Mancini, HL (2004). Uma Introdução à Ciência dos Materiais. Princeton University Press. ISBN 978-0-691-07097-1.
Ashby, Michael; Hugh Shercliff; David Cebon (2007). Materiais: engenharia, ciência, processamento e design (1ª ed.). Butterworth-Heinemann. ISBN 978-0-7506-8391-3.
JR Lamarsh, AJ Baratta, Introdução à Engenharia Nuclear, 3ª ed., Prentice-Hall, 2001, ISBN: 0-201-82498-1.
Esperamos que este artigo, Solid Solution Strengthening – Alloying, ajude você. Se sim, dê um like na barra lateral. O objetivo principal deste site é ajudar o público a aprender algumas informações interessantes e importantes sobre materiais e suas propriedades.