Carbono-14
El único radionúclido cosmogénico que hace una contribución significativa a la exposición interna del ser humano es el carbono 14. El carbono 14 radiactivo tiene una vida media de 5730 años y sufre desintegración β− , donde el neutrón se convierte en un protón , un electrón y un antineutrino electrónico :
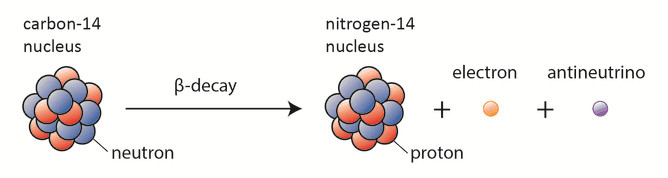
A pesar de esta corta vida media en comparación con la edad de la tierra, el carbono 14 es un isótopo natural. Su presencia puede explicarse mediante la siguiente simple observación. Nuestra atmósfera contiene muchos gases, incluido el nitrógeno 14. Además, la atmósfera es bombardeada constantemente con rayos cósmicos de alta energía , que consisten en protones, núcleos más pesados o rayos gamma. Estos rayos cósmicos interactúan con los núcleos de la atmósfera y producen también neutrones de alta energía . Estos neutrones producidos en estas colisiones pueden ser absorbidos por nitrógeno-14 para producir un isótopo de carbono-14:
El carbono 14 también se puede producir en la atmósfera mediante otras reacciones de neutrones, que incluyen en particular 13C (n, γ) 14C y 17O (n, α) 14C. Como resultado, el carbono 14 se forma continuamente en la atmósfera superior por la interacción de los rayos cósmicos con el nitrógeno atmosférico. En promedio, solo uno de cada 1.3 x 10 12 átomos de carbono en la atmósfera es un átomo de carbono 14 radiactivo. Como resultado, todas las sustancias biológicas vivas contienen la misma cantidad de C-14 por gramo de carbono, es decir, 0,3 Bq de actividad de carbono-14 por gramo de carbono. El carbono 14 está presente en el cuerpo humano (13 kg de carbono en 70 kg de ser humano) a un nivel de aproximadamente 3700 Bq (0,1 μCi) con una vida media biológica de 40 días. Tenga en cuenta que, la vida media biológicaes el tiempo que tarda la cantidad de un elemento en particular en el cuerpo en disminuir a la mitad de su valor inicial debido a la eliminación por procesos biológicos solamente. Sin embargo, un átomo de carbono está en la información genética de aproximadamente la mitad de las células, mientras que el potasio no es un componente del ADN. La desintegración de un átomo de carbono 14 dentro del ADN de una persona ocurre unas 50 veces por segundo, cambiando un átomo de carbono a uno de nitrógeno.
Se estima que la dosis anual de carbono 14 es de unos 12 μSv / año .
Mientras el sistema biológico esté vivo, el nivel es constante debido a la ingesta constante de todos los isótopos de carbono. Cuando el sistema biológico muere, deja de intercambiar carbono con su entorno y, a partir de ese momento, la cantidad de carbono 14 que contiene comienza a disminuir a medida que el carbono 14 sufre desintegración radiactiva.
Ver también: Datación por carbono-14
[/ lgc_column]
Protección de radiación:
- Knoll, Glenn F., Detección y medición de radiación, cuarta edición, Wiley, 8/2010. ISBN-13: 978-0470131480.
- Stabin, Michael G., Protección radiológica y dosimetría: Introducción a la física de la salud, Springer, 10/2010. ISBN-13: 978-1441923912.
- Martin, James E., Física para la protección radiológica, tercera edición, Wiley-VCH, 4/2013. ISBN-13: 978-3527411764.
- USNRC, CONCEPTOS DE REACTORES NUCLEARES
- Departamento de Energía, Física Nuclear y Teoría de Reactores de EE. UU. DOE Fundamentals Handbook, Volumen 1 y 2. Enero de 1993.
Física nuclear y de reactores:
- JR Lamarsh, Introducción a la teoría de los reactores nucleares, 2ª ed., Addison-Wesley, Reading, MA (1983).
- JR Lamarsh, AJ Baratta, Introducción a la ingeniería nuclear, 3d ed., Prentice-Hall, 2001, ISBN: 0-201-82498-1.
- WM Stacey, Física de reactores nucleares, John Wiley & Sons, 2001, ISBN: 0-471-39127-1.
- Glasstone, Sesonske. Ingeniería de Reactores Nucleares: Ingeniería de Sistemas de Reactores, Springer; 4a edición, 1994, ISBN: 978-0412985317
- WSC Williams. Física nuclear y de partículas. Prensa de Clarendon; 1 edición, 1991, ISBN: 978-0198520467
- GRKeepin. Física de la cinética nuclear. Addison-Wesley Pub. Co; 1a edición, 1965
- Robert Reed Burn, Introducción a la operación de reactores nucleares, 1988.
- Departamento de Energía, Física Nuclear y Teoría de Reactores de EE. UU. DOE Fundamentals Handbook, Volumen 1 y 2. Enero de 1993.
- Paul Reuss, Física de neutrones. EDP Sciences, 2008. ISBN: 978-2759800414.
[/ su_spoiler]
[/ lgc_column]Ver también:
Radionucleidos cosmogénicos [/ su_button] [/ lgc_column]
& nbsp;
Esperamos que este artículo, Carbono-14 - Producción - Propiedades - Decadencia , le ayude. Si es así, danos un me gusta en la barra lateral. El objetivo principal de este sitio web es ayudar al público a conocer información importante e interesante sobre los materiales y sus propiedades.