 Os metais leves e suas ligas são materiais de densidade relativamente baixa e altas relações resistência-peso. Esses metais e ligas são de grande importância em aplicações de engenharia para uso em transporte terrestre, marítimo, aéreo e espacial. Magnésio, alumínio e titânio são metais leves de significativa importância comercial. Esses três metais e suas ligas compreendem a maior parte dos materiais metálicos de alta relação resistência/peso usados em sistemas industriais. O alumínio é o mais versátil desses materiais e o titânio é o mais resistente à corrosão com resistência muito alta, enquanto o magnésio tem a densidade mais baixa. Suas densidades de 1,7 (magnésio), 2,7 (alumínio) e 4,5 g/cm3 (titânio) variam de 19 a 56% das densidades dos metais estruturais mais antigos, ferro (7,9 g/cm3) e cobre (8,9 g/cm3). Os metais comumente classificados como metais leves são aqueles cuja densidade é menor que a densidade do aço (7,8 g/cm3, ou 0,28 lb/in.3).
Os metais leves e suas ligas são materiais de densidade relativamente baixa e altas relações resistência-peso. Esses metais e ligas são de grande importância em aplicações de engenharia para uso em transporte terrestre, marítimo, aéreo e espacial. Magnésio, alumínio e titânio são metais leves de significativa importância comercial. Esses três metais e suas ligas compreendem a maior parte dos materiais metálicos de alta relação resistência/peso usados em sistemas industriais. O alumínio é o mais versátil desses materiais e o titânio é o mais resistente à corrosão com resistência muito alta, enquanto o magnésio tem a densidade mais baixa. Suas densidades de 1,7 (magnésio), 2,7 (alumínio) e 4,5 g/cm3 (titânio) variam de 19 a 56% das densidades dos metais estruturais mais antigos, ferro (7,9 g/cm3) e cobre (8,9 g/cm3). Os metais comumente classificados como metais leves são aqueles cuja densidade é menor que a densidade do aço (7,8 g/cm3, ou 0,28 lb/in.3).
Como esses metais puros são geralmente materiais mais macios com resistência insuficiente, eles devem ser ligados para atingir as propriedades mecânicas desejadas. Por exemplo, o alumínio de alta pureza é um material macio com resistência máxima de aproximadamente 10 MPa, o que limita sua usabilidade em aplicações industriais. Por outro lado, a resistência à tração da liga de alumínio 6061 pode atingir mais de 290 MPa, dependendo do temperamento do material. Portanto, estamos discutindo principalmente as ligas em vez de metais puros.
Densidade de metais leves e ligas
A densidade da liga de alumínio típica é de 2,7 g/cm3 (liga 6061).
A densidade da liga de magnésio típica é de 1,8 g/cm3 (Elektron 21).
A densidade da liga de titânio típica é de 4,43 g/cm3 (Ti-6Al-4V).
A densidade é definida como a massa por unidade de volume. É uma propriedade intensiva, que é matematicamente definida como massa dividida por volume:
ρ = m/V
Em palavras, a densidade (ρ) de uma substância é a massa total (m) dessa substância dividida pelo volume total (V) ocupado por essa substância. A unidade SI padrão é quilogramas por metro cúbico (kg/m3). A unidade padrão inglesa é libras-massa por pé cúbico (lbm/ft3).
Como a densidade (ρ) de uma substância é a massa total (m) dessa substância dividida pelo volume total (V) ocupado por essa substância, é óbvio que a densidade de uma substância depende fortemente de sua massa atômica e também de a densidade do número atômico (N; átomos/cm3),
- Peso Atômico. A massa atômica é transportada pelo núcleo atômico, que ocupa apenas cerca de 10-12 do volume total do átomo ou menos, mas contém toda a carga positiva e pelo menos 99,95% da massa total do átomo. Portanto, é determinado pelo número de massa (número de prótons e nêutrons).
- Densidade de Número Atômico. A densidade de número atômico (N; átomos/cm3), que está associada aos raios atômicos, é o número de átomos de um determinado tipo por unidade de volume (V; cm3) do material. A densidade do número atômico (N; átomos/cm3) de um material puro com peso atômico ou molecular (M; gramas/mol) e a densidade do material (⍴; grama/cm3) é facilmente calculada a partir da seguinte equação usando o número de Avogadro (NA = 6,022×1023 átomos ou moléculas por mol):
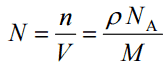
- Estrutura de cristal. A densidade da substância cristalina é significativamente afetada por sua estrutura cristalina. A estrutura FCC, junto com seu parente hexagonal (hcp), tem o fator de empacotamento mais eficiente (74%). Metais contendo estruturas FCC incluem austenita, alumínio, cobre, chumbo, prata, ouro, níquel, platina e tório.
Departamento de Energia dos EUA, Ciência de Materiais. DOE Fundamentals Handbook, Volume 1 e 2. Janeiro de 1993.
Departamento de Energia dos EUA, Ciência de Materiais. DOE Fundamentals Handbook, Volume 2 e 2. Janeiro de 1993.
William D. Callister, David G. Rethwisch. Ciência e Engenharia de Materiais: Uma Introdução 9ª Edição, Wiley; 9 edição (4 de dezembro de 2013), ISBN-13: 978-1118324578.
Eberhart, Mark (2003). Por que as coisas quebram: entendendo o mundo pela maneira como ele se desfaz. Harmonia. ISBN 978-1-4000-4760-4.
Gaskell, David R. (1995). Introdução à Termodinâmica dos Materiais (4ª ed.). Editora Taylor e Francis. ISBN 978-1-56032-992-3.
González-Viñas, W. & Mancini, HL (2004). Uma Introdução à Ciência dos Materiais. Princeton University Press. ISBN 978-0-691-07097-1.
Ashby, Michael; Hugh Shercliff; David Cebon (2007). Materiais: engenharia, ciência, processamento e design (1ª ed.). Butterworth-Heinemann. ISBN 978-0-7506-8391-3.
JR Lamarsh, AJ Baratta, Introdução à Engenharia Nuclear, 3ª ed., Prentice-Hall, 2001, ISBN: 0-201-82498-1.
Esperamos que este artigo, Densidade de metais leves e ligas, ajude você. Se sim, dê um like na barra lateral. O objetivo principal deste site é ajudar o público a aprender algumas informações interessantes e importantes sobre materiais e suas propriedades.