Un enlace químico es una atracción duradera entre estos átomos, iones o moléculas que permite la formación de compuestos químicos. El enlace puede resultar de la fuerza de atracción electrostática entre iones con carga opuesta, como en los enlaces iónicos, o mediante el intercambio de electrones, como en los enlaces covalentes. Por lo tanto, la fuerza electromagnética juega un papel importante en la determinación de las propiedades internas de la mayoría de los objetos que se encuentran en la vida diaria.
Enlace covalente
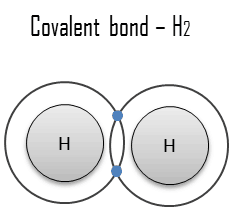 Un enlace covalente es un enlace químico formado por electrones compartidos . Los electrones de valencia se comparten cuando un átomo necesita electrones para completar su capa exterior y puede compartir esos electrones con su vecino. Los electrones son entonces parte de ambos átomos y ambas capas se llenan. Estos pares de electrones se conocen como pares compartidos o pares de enlace , y el equilibrio estable de fuerzas atractivas y repulsivas entre átomos, cuando comparten electrones, se conoce como enlace covalente .
Un enlace covalente es un enlace químico formado por electrones compartidos . Los electrones de valencia se comparten cuando un átomo necesita electrones para completar su capa exterior y puede compartir esos electrones con su vecino. Los electrones son entonces parte de ambos átomos y ambas capas se llenan. Estos pares de electrones se conocen como pares compartidos o pares de enlace , y el equilibrio estable de fuerzas atractivas y repulsivas entre átomos, cuando comparten electrones, se conoce como enlace covalente .
El tipo más simple y común es un enlace sencillo en el que dos átomos comparten dos electrones. Otros tipos incluyen el enlace doble (por ejemplo, H 2 C = CH 2 ), el enlace triple, enlaces de uno y tres electrones, enlace de dos electrones de tres centros y enlace de cuatro electrones de tres centros.
La covalencia es máxima entre átomos de electronegatividades similares . Por lo tanto, el enlace covalente no requiere necesariamente que los dos átomos sean de los mismos elementos, solo que tengan una electronegatividad comparable (es decir, elementos que se encuentran cerca uno del otro en la tabla periódica ). No existe un valor preciso que distinga los enlaces iónicos de los covalentes, pero es probable que una diferencia de electronegatividad de más de 1,7 sea iónica, mientras que una diferencia de menos de 1,7 sea covalente.
[/ lgc_column]
Ciencia de los materiales:
- Departamento de Energía de EE. UU., Ciencia de Materiales. DOE Fundamentals Handbook, Volumen 1 y 2. Enero de 1993.
- Departamento de Energía de EE. UU., Ciencia de Materiales. DOE Fundamentals Handbook, Volumen 2 y 2. Enero de 1993.
- William D. Callister, David G. Rethwisch. Ciencia e Ingeniería de Materiales: Introducción 9ª Edición, Wiley; 9a edición (4 de diciembre de 2013), ISBN-13: 978-1118324578.
- Eberhart, Mark (2003). Por qué se rompen las cosas: comprender el mundo a través de la forma en que se desmorona. Armonía. ISBN 978-1-4000-4760-4.
- Gaskell, David R. (1995). Introducción a la Termodinámica de Materiales (4ª ed.). Taylor y Francis Publishing. ISBN 978-1-56032-992-3.
- González-Viñas, W. y Mancini, HL (2004). Introducción a la ciencia de los materiales. Prensa de la Universidad de Princeton. ISBN 978-0-691-07097-1.
- Ashby, Michael; Hugh Shercliff; David Cebon (2007). Materiales: ingeniería, ciencia, procesamiento y diseño (1ª ed.). Butterworth-Heinemann. ISBN 978-0-7506-8391-3.
- JR Lamarsh, AJ Baratta, Introducción a la ingeniería nuclear, 3d ed., Prentice-Hall, 2001, ISBN: 0-201-82498-1.
[/ su_spoiler] [/ su_accordion]
[/ lgc_column]Véase más arriba:
Enlace químico [/ su_button] [/ lgc_column]
Esperamos que este artículo, Covalent bond , te ayude. Si es así, danos un me gusta en la barra lateral. El objetivo principal de este sitio web es ayudar al público a conocer información importante e interesante sobre los materiales y sus propiedades.