Cet article contient une comparaison des principales propriétés thermiques et atomiques de l’iode et du mercure, deux éléments chimiques comparables du tableau périodique. Il contient également des descriptions de base et des applications des deux éléments. Iode contre Mercure.
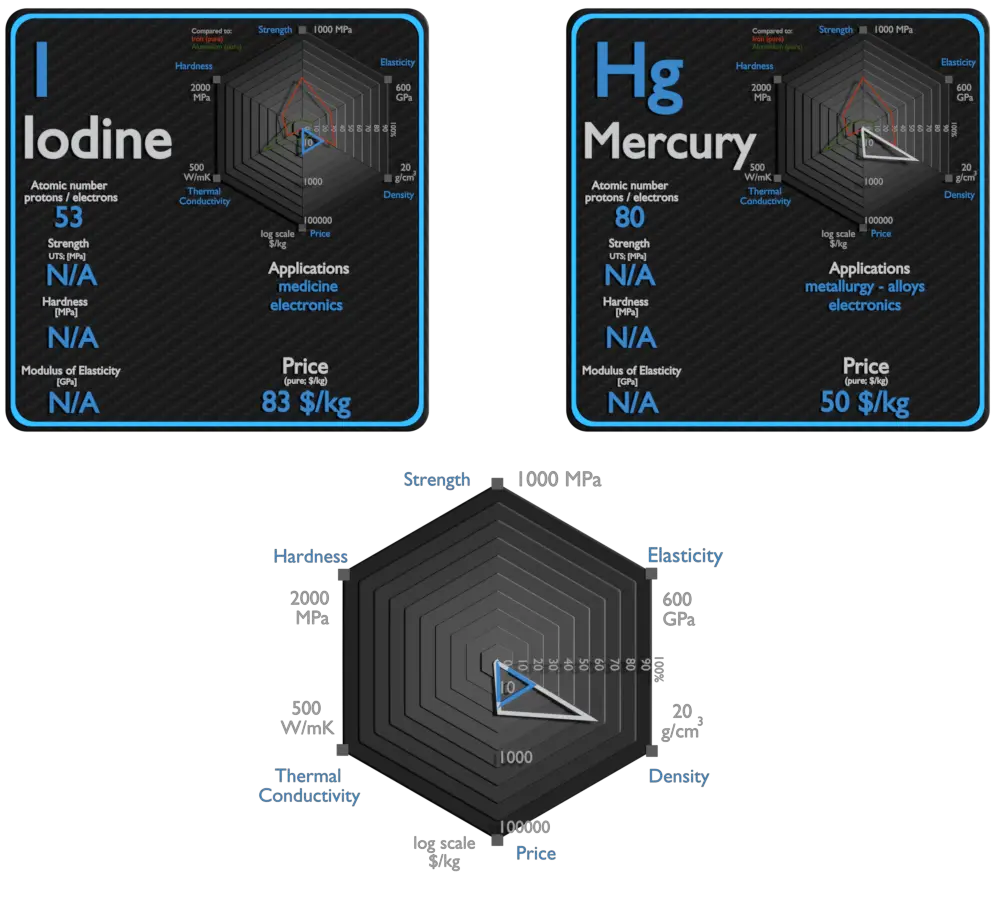
L’iode et le Mercure – À propos des éléments


Source : www.luciteria.com
Iode et Mercure – Applications
Iode
En plus des produits nutritionnels, l’iode et les dérivés d’iode sont utilisés dans un large éventail d’applications médicales, agricoles et industrielles. Environ la moitié de tout l’iode produit entre dans divers composés organoiodés, 15% restants restent sous forme d’élément pur, 15% supplémentaires sont utilisés pour former de l’iodure de potassium et 15% supplémentaires pour d’autres composés iodés inorganiques. L’application principale est la production de produits de contraste pour rayons X (22 %). Le numéro atomique et la densité élevés de l’iode le rendent parfaitement adapté à cette application, car sa présence dans le corps peut aider à augmenter le contraste entre les tissus, les organes et les vaisseaux sanguins avec des densités de rayons X similaires. Il est utilisé comme antiseptique pour les plaies externes. Une autre application à l’origine de la demande d’iode est le film polarisant dans les écrans à cristaux liquides (LCD).
Mercure
Le mercure est principalement utilisé pour la fabrication de produits chimiques industriels ou pour des applications électriques et électroniques. Cependant, en raison de sa toxicité, de nombreuses utilisations du mercure sont en cours d’élimination ou sont en cours de révision. Il est utilisé dans certains thermomètres, en particulier ceux qui sont utilisés pour mesurer des températures élevées. Le mercure forme facilement des alliages, appelés amalgames, avec d’autres métaux tels que l’or, l’argent et l’étain. La facilité avec laquelle il s’amalgame avec l’or le rend utile pour récupérer l’or de ses minerais. Les amalgames au mercure étaient également utilisés dans les obturations dentaires. Le mercure gazeux est utilisé dans les lampes à vapeur de mercure et certaines enseignes publicitaires de type « enseigne au néon » et lampes fluorescentes.
Iode et Mercure – Comparaison dans le tableau
| Élément | Iode | Mercure |
| Densité | 4,94 g/cm3 | 13,534 g/cm3 |
| Résistance à la traction ultime | N / A | N / A |
| Limite d’élasticité | N / A | N / A |
| Module de Young | N / A | N / A |
| Échelle de Mohs | N / A | N / A |
| Dureté Brinell | N / A | N / A |
| Dureté Vickers | N / A | N / A |
| Point de fusion | 113,5 °C | -38,9 °C |
| Point d’ébullition | 184 °C | 357 °C |
| Conductivité thermique | 0,449 W/mK | 8,3 W/mK |
| Coefficient de dilatation thermique | N / A | 60,4 µm/mK |
| Chaleur spécifique | 0,214 J/g·K | 0,139 J/g·K |
| Température de fusion | 7,824 kJ/mol | 2,295 kJ/mole |
| Chaleur de vaporisation | 20,752 kJ/mole | 59,229 kJ/mol |









