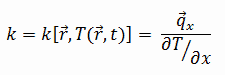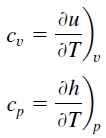Acerca del dióxido de carbono
El dióxido de carbono es un gas incoloro con una densidad aproximadamente un 53% más alta que la del aire seco. Es relativamente no tóxico y no combustible, pero es más pesado que el aire y puede asfixiarse por el desplazamiento del aire. Cuando el CO2 se disuelve en agua, se forma el ácido carbónico suave. El CO2 enfriado en forma sólida se llama hielo seco. El dióxido de carbono es un componente menor de la atmósfera terrestre, pero un componente importante del aire. Es una materia prima necesaria para la mayoría de las plantas, que eliminan el dióxido de carbono del aire mediante el proceso de fotosíntesis. Una concentración típica de CO2 en el aire es actualmente de aproximadamente 0,040% o 404 ppm. La concentración de dióxido de carbono atmosférico aumenta y disminuye en un patrón estacional en un rango de aproximadamente 6 ppmv. La concentración de CO2 en el aire también ha aumentado constantemente de año durante más de 70 años. La tasa actual de aumento es de aproximadamente 2,5 ppm por año.

Resumen
| Nombre | Dióxido de carbono |
| Fase en STP | gaseoso |
| Densidad | 2 kg / m 3 |
| Resistencia a la tracción | N / A |
| Límite de elastacidad | N / A |
| Módulo de Young | N / A |
| Dureza Brinell | N / A |
| Punto de fusión | -57 ° C |
| Conductividad térmica | 0,0166 W / mK |
| Capacidad calorífica | 840 J / g K |
| Precio | 2 $ / kg |
Densidad de dióxido de carbono
Las densidades típicas de varias sustancias se encuentran a presión atmosférica. La densidad se define como la masa por unidad de volumen . Es una propiedad intensiva , que se define matemáticamente como masa dividida por volumen: ρ = m / V
En palabras, la densidad (ρ) de una sustancia es la masa total (m) de esa sustancia dividida por el volumen total (V) ocupado por esa sustancia. La unidad estándar del SI es kilogramos por metro cúbico ( kg / m 3 ). La unidad de inglés estándar es libras de masa por pie cúbico ( lbm / ft 3 ).
La densidad del dióxido de carbono es de 2 kg / m 3 .
Densidad de materiales
Propiedades térmicas del dióxido de carbono
Dióxido de carbono – Punto de fusión
Punto de Dióxido de Carbono de fusión es de -57 ° C .
Tenga en cuenta que estos puntos están asociados con la presión atmosférica estándar. En general, la fusión es un cambio de fase de una sustancia de la fase sólida a la líquida. El punto de fusión de una sustancia es la temperatura a la que se produce este cambio de fase. El punto de fusión también define una condición en la que el sólido y el líquido pueden existir en equilibrio. Para varios compuestos químicos y aleaciones, es difícil definir el punto de fusión, ya que generalmente son una mezcla de varios elementos químicos.
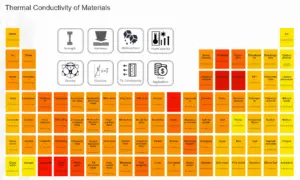
Dióxido de carbono: conductividad térmica
La conductividad térmica del dióxido de carbono es 0,0166 W / (m · K) .
Las características de transferencia de calor de un material sólido se miden mediante una propiedad llamada conductividad térmica , k (o λ), medida en W / mK . Es una medida de la capacidad de una sustancia para transferir calor a través de un material por conducción . Tenga en cuenta que la ley de Fourier se aplica a toda la materia, independientemente de su estado (sólido, líquido o gas), por lo tanto, también se define para líquidos y gases.
La conductividad térmica de la mayoría de los líquidos y variadas con la temperatura. Para los vapores, también depende de la presión. En general:
La mayoría de los materiales son casi homogéneos, por lo que normalmente podemos escribir k = k (T) . Se asocian definiciones similares con conductividades térmicas en las direcciones yyz (ky, kz), pero para un material isótropo, la conductividad térmica es independiente de la dirección de transferencia, kx = ky = kz = k.
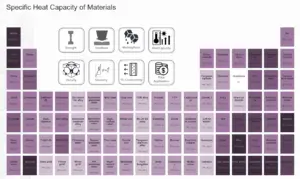
Dióxido de carbono – Calor específico
El calor Específico de Dióxido de Carbono es de 840 J / g K .
El calor específico, o capacidad calorífica específica, es una propiedad relacionada con la energía interna que es muy importante en termodinámica. Las propiedades intensivas c v y c p se definen para sustancias compresibles simples puras como derivadas parciales de la energía interna u (T, v) y la entalpía h (T, p) , respectivamente:
donde los subíndices v y p significan las variables mantiene fijo durante la diferenciación. Las propiedades c v y c p se conocen como calores específicas (o capacidades caloríficas ) porque bajo ciertas condiciones especiales relacionan el cambio de temperatura de un sistema con la cantidad de energía agregada por la transferencia de calor. Unidades Sus SI hijo J / kg K o J / K mol .