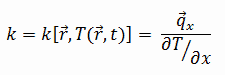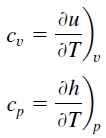Sobre el grafito
El grafito es una forma cristalina del elemento carbono con sus átomos dispuestos en una estructura hexagonal. Su combinación poco común de propiedades se debe a la estructura cristalina del grafito. Los átomos de carbono se colocan hexagonalmente en un sistema de anillo condensado plano. Las capas se apilan paralelas entre sí. Los átomos dentro de los anillos están unidos de forma covalente, mientras que las capas están unidas entre sí por las fuerzas de van der Waals. Ocurre naturalmente en esta forma y es la forma más estable de carbono en condiciones estándar. Aunque el grafito es flexible, no es elástico y tiene una alta conductividad eléctrica y térmica. También es químicamente inerte y altamente refractario. Dado que el grafito presenta una baja adsorción de rayos X y neutrones, es muy valioso en aplicaciones nucleares.
Resumen
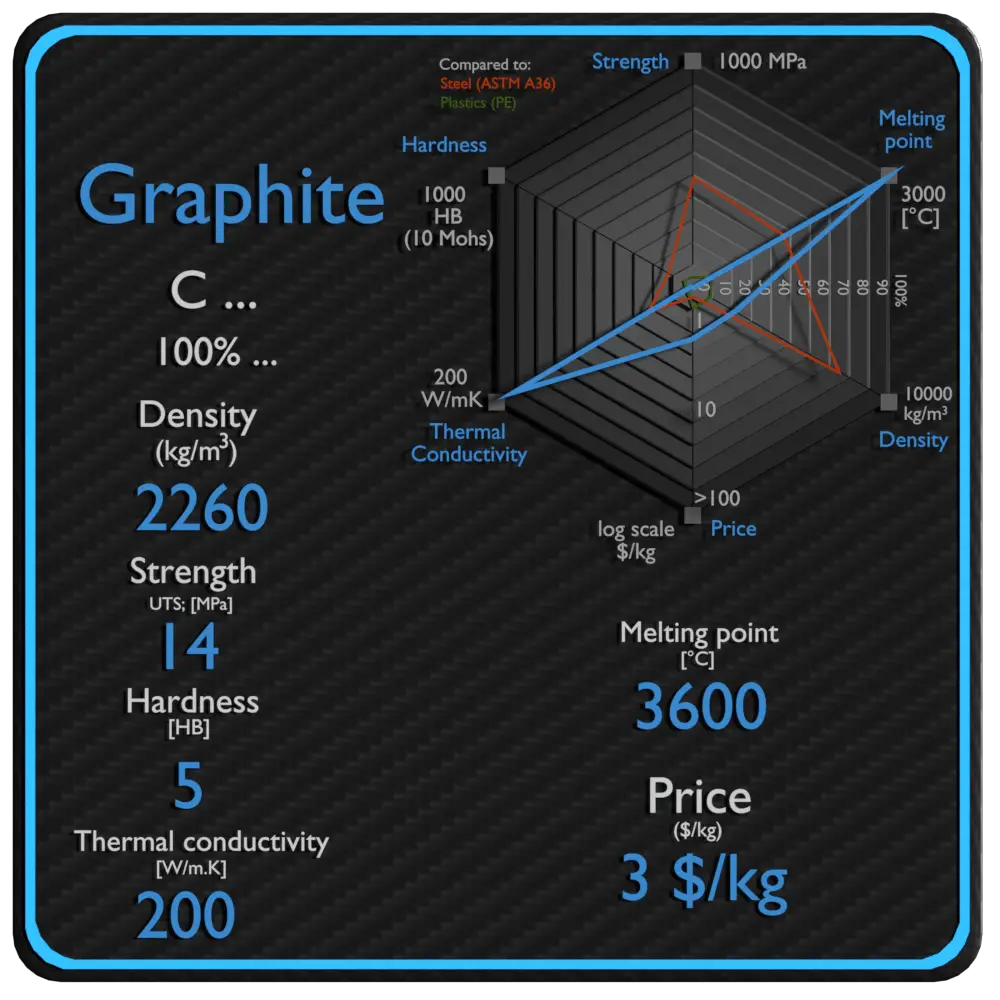
| Nombre | Grafito |
| Fase en STP | sólido |
| Densidad | 2260 kg / m3 |
| Resistencia a la tracción | 14 MPa |
| Límite de elastacidad | N / A |
| Módulo de Young | 11,5 GPa |
| Dureza Brinell | 5 BHN |
| Punto de fusión | 3600 ° C |
| Conductividad térmica | 200 W / mK |
| Capacidad calorífica | 720 J / g K |
| Precio | 3 $ / kg |
Composición de grafito
Su combinación poco común de propiedades se debe a la estructura cristalina del grafito. Los átomos de carbono se colocan hexagonalmente en un sistema de anillo condensado plano. Las capas se apilan paralelas entre sí. Los átomos dentro de los anillos están unidos de forma covalente, mientras que las capas están unidas entre sí por las fuerzas de van der Waals. Ocurre naturalmente en esta forma y es la forma más estable de carbono en condiciones estándar.
Aplicaciones del grafito

Las propiedades del grafito determinan la variedad de áreas de sus aplicaciones en la industria, transporte, energética, defensa, medicina, ciencia, deporte. Debido a su estabilidad a altas temperaturas e inercia química, el grafito es el candidato perfecto para material refractario. Según el USGS, el consumo de grafito natural en los Estados Unidos en los refractarios fue de 12.500 toneladas en 2010. Las escobillas de carbón para motores eléctricos se fabrican con grafito sintético de alta pureza. El grafito de alta pureza también se utiliza en reactores nucleares como moderador de neutrones. Esto se debe a su sección transversal de muy baja absorción. El grafito natural en la fabricación de acero se utiliza principalmente para aumentar el contenido de carbono en el acero fundido.
Propiedades térmicas del grafito
Grafito – Punto de fusión
Punto de grafito de fusión es de 3600 ° C .
Tenga en cuenta que estos puntos están asociados con la presión atmosférica estándar. En general, la fusión es un cambio de fase de una sustancia de la fase sólida a la líquida. El punto de fusión de una sustancia es la temperatura a la que se produce este cambio de fase. El punto de fusión también define una condición en la que el sólido y el líquido pueden existir en equilibrio. Para varios compuestos químicos y aleaciones, es difícil definir el punto de fusión, ya que generalmente son una mezcla de varios elementos químicos.
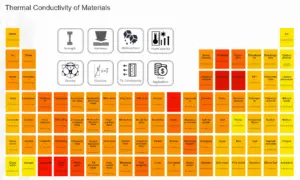
Grafito – Conductividad térmica
La conductividad térmica del grafito es 200 W / (m · K) .
Las características de transferencia de calor de un material sólido se miden mediante una propiedad llamada conductividad térmica , k (o λ), medida en W / mK . Es una medida de la capacidad de una sustancia para transferir calor a través de un material por conducción . Tenga en cuenta que la ley de Fourier se aplica a toda la materia, independientemente de su estado (sólido, líquido o gas), por lo que también se define para líquidos y gases.
La conductividad térmica de la mayoría de los líquidos y sólidos varía con la temperatura. Para los vapores, también depende de la presión. En general:
La mayoría de los materiales son casi homogéneos, por lo que normalmente podemos escribir k = k (T) . Se asocian definiciones similares con las conductividades térmicas en las direcciones y y z (ky, kz), pero para un material isótropo, la conductividad térmica es independiente de la dirección de transferencia, kx = ky = kz = k.
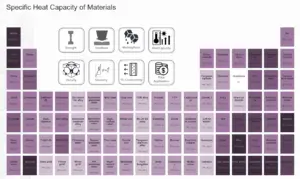
Grafito – Calor específico
Calor específico del grafito es de 720 J / g K .
El calor específico, o capacidad calorífica específica, es una propiedad relacionada con la energía interna que es muy importante en termodinámica. Las propiedades intensivas c v y c p se definen para sustancias compresibles simples puras como derivadas parciales de la energía interna u (T, v) y la entalpía h (T, p) , respectivamente:
donde los subíndices v y p denotan las variables que se mantienen fijas durante la diferenciación. Las propiedades c v y c p se denominan calores específicos (o capacidades caloríficas ) porque, en determinadas condiciones especiales, relacionan el cambio de temperatura de un sistema con la cantidad de energía añadida por la transferencia de calor. Sus unidades SI son J / kg K o J / mol K .
Propiedades y precios de otros materiales
tabla-de-materiales-en-resolución-8k