Cet article contient une comparaison des principales propriétés thermiques et atomiques du brome et de l’iode, deux éléments chimiques comparables du tableau périodique. Il contient également des descriptions de base et des applications des deux éléments. Brome vs Iode.
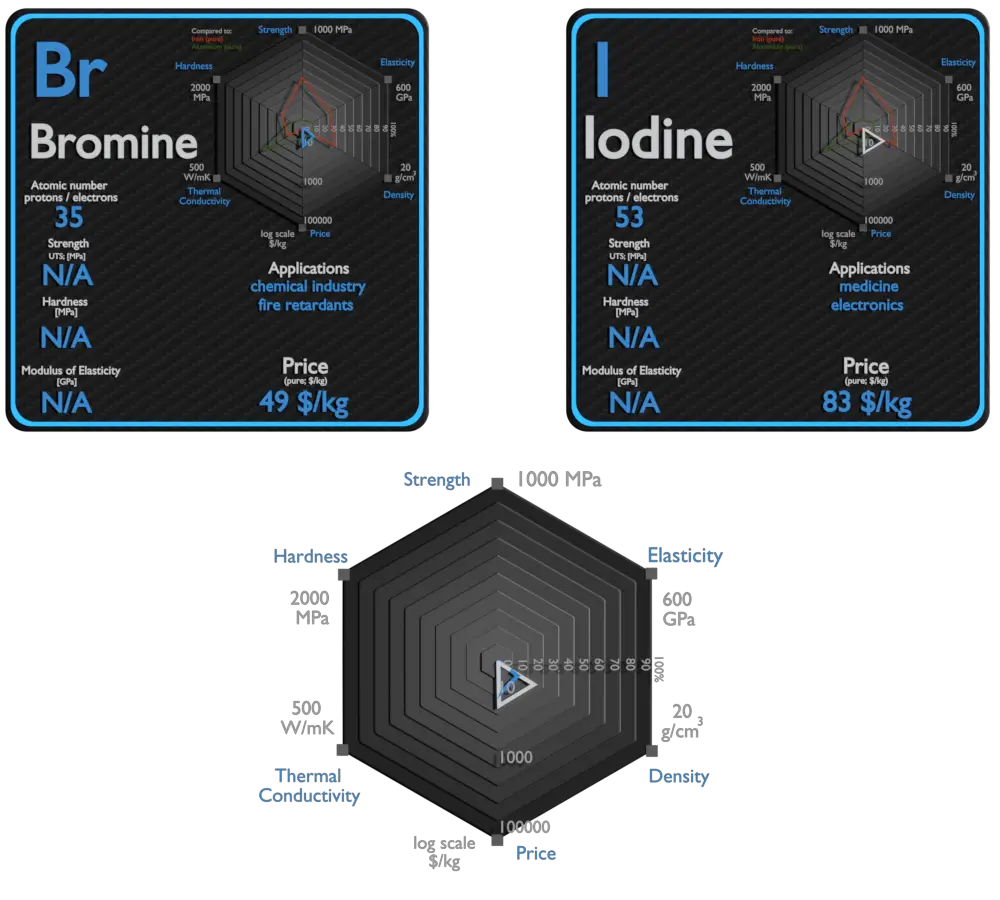
Brome et Iode – À propos des éléments


Source : www.luciteria.com
Brome et Iode – Applications
Brome
Une grande variété de composés organobromés sont utilisés dans l’industrie. Certains sont préparés à partir de brome et d’autres sont préparés à partir de bromure d’hydrogène, qui est obtenu en brûlant de l’hydrogène dans du brome. Les retardateurs de flamme bromés représentent un produit d’importance croissante et constituent la plus grande utilisation commerciale du brome. L’une des principales utilisations du brome est un purificateur/désinfectant de l’eau, comme alternative au chlore. Les composés de brome sont des pesticides efficaces, utilisés à la fois comme fumigants du sol dans l’agriculture, en particulier la culture fruitière, et comme fumigants pour empêcher les ravageurs d’attaquer les céréales stockées et d’autres produits.
Iode
En plus des produits nutritionnels, l’iode et les dérivés d’iode sont utilisés dans un large éventail d’applications médicales, agricoles et industrielles. Environ la moitié de tout l’iode produit entre dans divers composés organoiodés, 15% restants restent sous forme d’élément pur, 15% supplémentaires sont utilisés pour former de l’iodure de potassium et 15% supplémentaires pour d’autres composés iodés inorganiques. L’application principale est la production de produits de contraste pour rayons X (22 %). Le numéro atomique et la densité élevés de l’iode le rendent parfaitement adapté à cette application, car sa présence dans le corps peut aider à augmenter le contraste entre les tissus, les organes et les vaisseaux sanguins avec des densités de rayons X similaires. Il est utilisé comme antiseptique pour les plaies externes. Une autre application à l’origine de la demande d’iode est le film polarisant dans les écrans à cristaux liquides (LCD).
Brome et Iode – Comparaison dans le tableau
| Élément | Brome | Iode |
| Densité | 3,12 g/cm3 | 4,94 g/cm3 |
| Résistance à la traction ultime | N / A | N / A |
| Limite d’élasticité | N / A | N / A |
| Module d’élasticité de Young | N / A | N / A |
| Échelle de Mohs | N / A | N / A |
| Dureté Brinell | N / A | N / A |
| Dureté Vickers | N / A | N / A |
| Point de fusion | -7,3°C | 113,5°C |
| Point d’ébullition | 59°C | 184°C |
| Conductivité thermique | 0,122 W/mK | 0,449 W/mK |
| Coefficient de dilatation thermique | N / A | N / A |
| Chaleur spécifique | 0,473 J/g·K | 0,214 J/g·K |
| Température de fusion | 5,286 kJ/mol | 7,824 kJ/mol |
| Chaleur de vaporisation | 15,438 kJ/mol | 20,752 kJ/mole |










