Cet article contient une comparaison des principales propriétés thermiques et atomiques de l’hydrogène et du calcium, deux éléments chimiques comparables du tableau périodique. Il contient également des descriptions de base et des applications des deux éléments. Hydrogène vs Calcium.
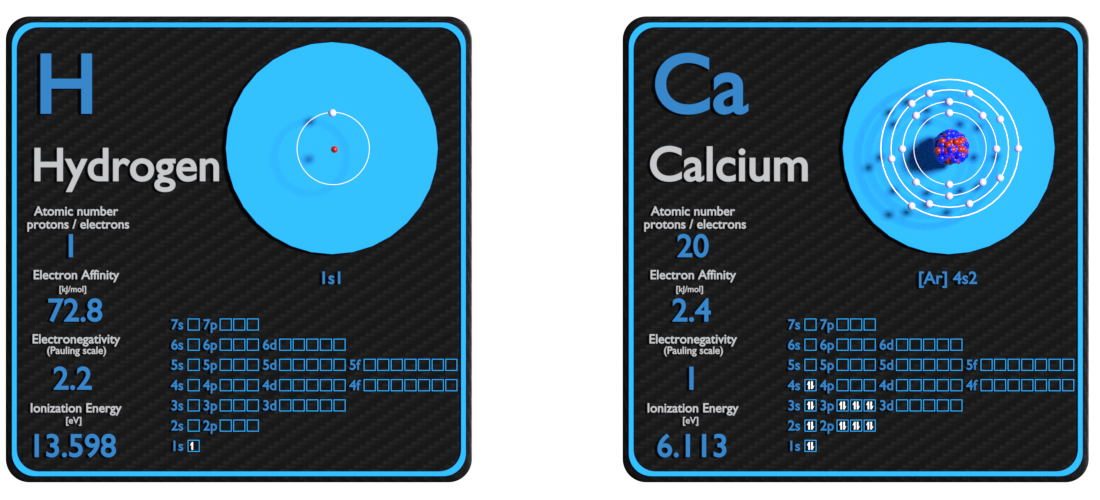
L’hydrogène et le Calcium – À propos des éléments


Source : www.luciteria.com
Hydrogène et Calcium – Applications
Hydrogène
L’hydrogène est polyvalent et peut être utilisé de différentes manières. Ces usages multiples peuvent être regroupés en deux grandes catégories. L’hydrogène comme matière première. Un rôle dont l’importance est reconnue depuis des décennies et qui continuera de croître et d’évoluer. La plus grande utilisation unique d’hydrogène dans le monde est la fabrication d’ammoniac, qui consomme environ les deux tiers de la production mondiale d’hydrogène. L’hydrogène est polyvalent et peut être utilisé de différentes manières. Ces usages multiples peuvent être regroupés en deux grandes catégories. L’hydrogène comme matière première pour d’autres procédés chimiques. Un rôle dont l’importance est reconnue depuis des décennies et qui continuera de croître et d’évoluer. Et l’hydrogène comme vecteur énergétique.
Calcium
La plus grande utilisation de calcium métallique est dans la sidérurgie, en raison de sa forte affinité chimique pour l’oxygène et le soufre. Ses oxydes et sulfures, une fois formés, donnent des inclusions d’aluminate de chaux liquide et de sulfure dans l’acier qui flottent. Les composés de calcium sont utilisés dans la fabrication d’insecticides, de peintures, de craie à tableau noir, de textiles et de feux d’artifice.
Hydrogène et Calcium – Comparaison dans le tableau
| Élément | Hydrogène | Calcium |
| Densité | 0,00009 g/cm3 | 1,55 g/cm3 |
| Résistance à la traction ultime | N / A | 110 MPa |
| Limite d’élasticité | N / A | N / A |
| Module de Young | N / A | 20 GPa |
| Échelle de Mohs | N / A | 1,5 |
| Dureté Brinell | N / A | 170 – 400 MPa |
| Dureté Vickers | N / A | N / A |
| Point de fusion | -259,1 °C | 842 °C |
| Point d’ébullition | -252,9 °C | 1484 °C |
| Conductivité thermique | 0,1805 W/mK | 200W/mK |
| Coefficient de dilatation thermique | N / A | 22,3 µm/mK |
| Chaleur spécifique | 14.304 J/g·K | 0,63 J/g·K |
| Température de fusion | 0,05868 kJ/mol | 8,54 kJ/mol |
| Chaleur de vaporisation | 0,44936 kJ/mol | 153,3 kJ/mol |