Este artigo contém uma comparação das principais propriedades térmicas e atômicas do irídio e da platina, dois elementos químicos comparáveis da tabela periódica. Ele também contém descrições básicas e aplicações de ambos os elementos. Iridium vs. Platinum.
Irídio e Platina – Sobre Elementos


Fonte: www.luciteria.com
Iridium e Platinum – Aplicações
Irídio
O irídio é consumido principalmente pelas indústrias automotiva, eletrônica e química. O irídio metálico é empregado quando é necessária alta resistência à corrosão em altas temperaturas, como em velas de ignição de alto desempenho, cadinhos para recristalização de semicondutores em altas temperaturas e eletrodos para a produção de cloro no processo cloroálcali. A demanda por irídio aumentou de 2,5 toneladas em 2009 para 10,4 toneladas em 2010, principalmente por causa de aplicações relacionadas à eletrônica que viram um aumento de 0,2 para 6 toneladas – os cadinhos de irídio são comumente usados para o cultivo de grandes cristais únicos de alta qualidade, cuja demanda aumentou acentuadamente.
Platina
A platina é principalmente um metal industrial. É um material crítico para muitas indústrias e é considerado um metal estratégico. A platina é usada como catalisador, a platina é encontrada principalmente em conversores catalíticos de veículos que reduzem produtos químicos tóxicos de exaustão e também em células de combustível para aumentar a eficiência. O uso mais comum da platina é como catalisador em reações químicas, muitas vezes como negro de platina. Nos conversores catalíticos, a platina permite a combustão completa de baixas concentrações de hidrocarbonetos não queimados do escape em dióxido de carbono e vapor de água. A platina tem sido usada em dispositivos termopares que medem a temperatura com alta precisão. A platina é um componente em revestimentos magnéticos para unidades de disco rígido de alta densidade e alguns dos sistemas de armazenamento óptico mais recentes.
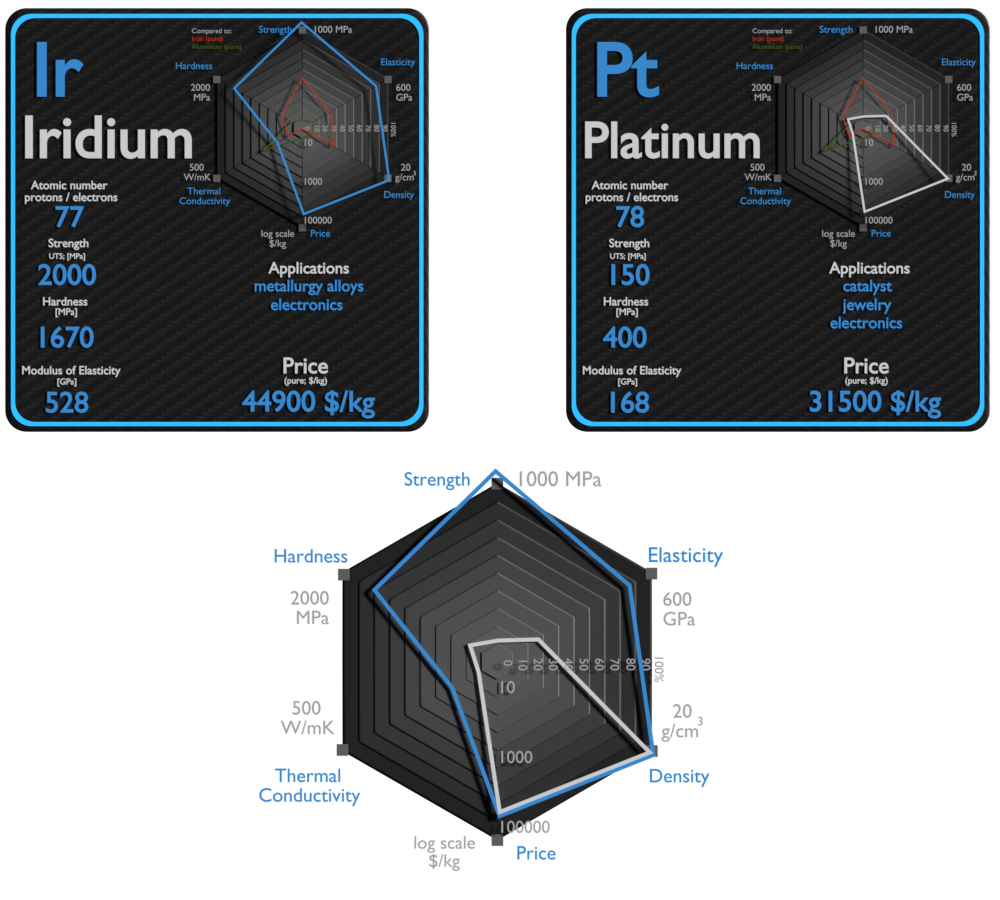
Irídio e Platina – Comparação na Tabela
| Elemento | Irídio | Platina |
| Densidade | 22,65 g/cm3 | 21,09 g/cm3 |
| Resistência à tração | 2000 MPa | 150 MPa |
| Força de rendimento | N/D | 70 MPa |
| Módulo de elasticidade de Young | 528 GPa | 168 GPa |
| Escala de Mohs | 6,25 | 3,5 |
| Dureza Brinell | 1670 MPa | 400 MPa |
| Dureza Vickers | 1760 MPa | 550 MPa |
| Ponto de fusão | 2410 °C | 1772 °C |
| Ponto de ebulição | 4130 °C | 3827 °C |
| Condutividade térmica | 150 W/mK | 72 W/mK |
| Coeficiente de Expansão Térmica | 6,4 µm/mK | 8,8 µm/mK |
| Calor específico | 0,13 J/gK | 0,13 J/gK |
| Calor de fusão | 26,1 kJ/mol | 19,6 kJ/mol |
| Calor da vaporização | 604 kJ/mol | 510 kJ/mol |








