Este artículo contiene una comparación de las propiedades térmicas y atómicas clave del magnesio y el potasio, dos elementos químicos comparables de la tabla periódica. También contiene descripciones básicas y aplicaciones de ambos elementos. Magnesio vs Potasio.
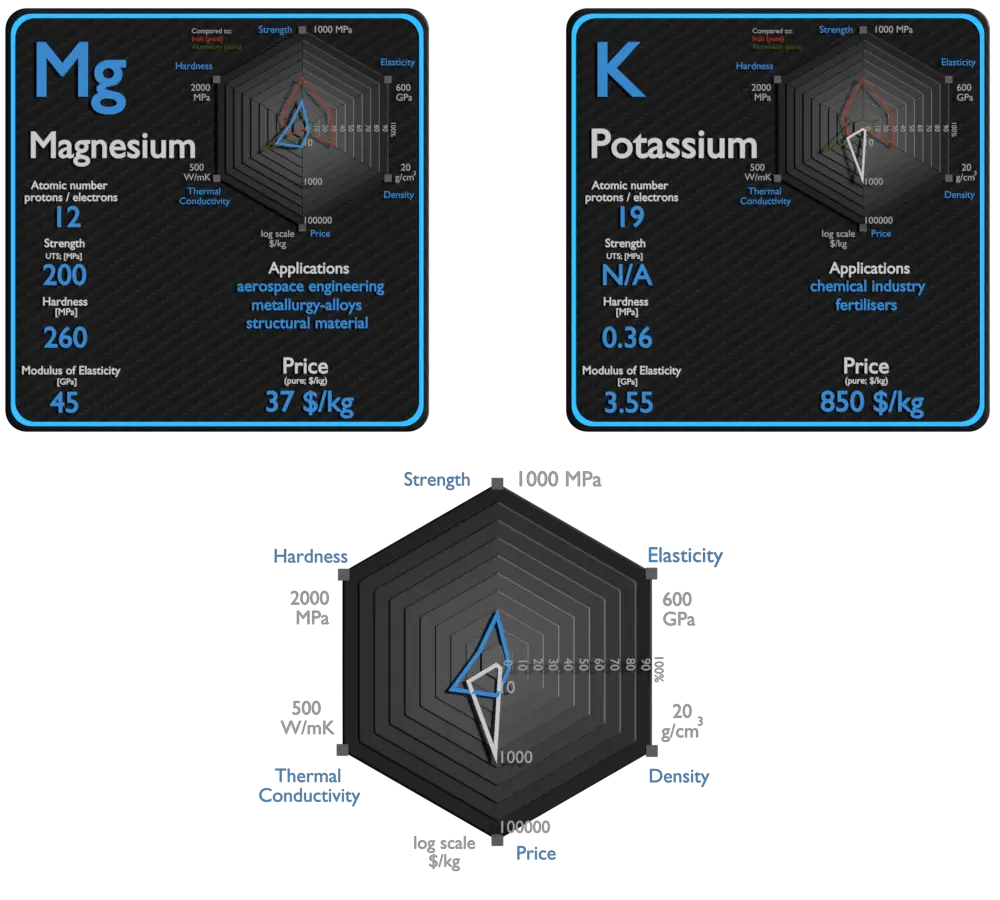
Magnesio y Potasio: acerca de los elementos


Fuente: www.luciteria.com
Magnesio y Potasio: aplicaciones
Magnesio
El magnesio es el tercer metal estructural más utilizado, después del hierro y el aluminio. [35] Las principales aplicaciones del magnesio son, en orden: aleaciones de aluminio, fundición a presión (aleado con zinc), eliminación de azufre en la producción de hierro y acero, y producción de titanio en el proceso Kroll. Las aleaciones de magnesio se utilizan en una amplia variedad de aplicaciones estructurales y no estructurales. Las aplicaciones estructurales incluyen equipos automotrices, industriales, de manipulación de materiales, comerciales y aeroespaciales. Las aleaciones de magnesio se utilizan para piezas que funcionan a altas velocidades y, por lo tanto, deben ser livianas para minimizar las fuerzas de inercia. Las aplicaciones comerciales incluyen herramientas de mano, computadoras portátiles, equipaje y escaleras, automóviles (por ejemplo, volantes y columnas, armazones de asientos, cajas de transmisión). Magnox (aleación),
Potasio
El potasio (K) es un nutriente esencial para el crecimiento de las plantas. Se clasifica como macronutriente porque las plantas absorben grandes cantidades de K durante su ciclo de vida. Los fertilizantes agrícolas consumen el 95% de la producción química mundial de potasio, y aproximadamente el 90% de este potasio se suministra como KCl. Debido a su alto grado de reactividad, el potasio puro rara vez se usa en su forma elemental / metálica. Se utiliza como un poderoso agente reductor en química orgánica. Las aleaciones de potasio / sodio se utilizan como medio de intercambio de calor. El calor del potasio calienta el agua y la calienta lo suficiente como para hervir. Luego, el agua se convierte en vapor, que se utiliza para hacer funcionar los dispositivos que generan electricidad.
Magnesio y Potasio: comparación en la tabla
| Elemento | Magnesio | Potasio |
| Densidad | 1,738 g / cm3 | 0,856 g / cm3 |
| Resistencia a la tracción | 200 MPa | N / A |
| Límite de elastacidad | N / A | N / A |
| Módulo de Young | 45 GPa | 3,53 GPa |
| Escala de Mohs | 2,5 | 0,4 |
| Dureza Brinell | 260 MPa | 0,36 MPa |
| Dureza Vickers | N / A | N / A |
| Punto de fusion | 649 ° C | 63,25 ° C |
| Punto de ebullición | 1090 ° C | 760 ° C |
| Conductividad térmica | 156 W / mK | 102,4 W / mK |
| Coeficiente de expansión térmica | 24,8 µm / mK | 83 µm / mK |
| Calor especifico | 1,02 J / g K | 0,75 J / g K |
| Calor de fusión | 8,954 kJ / mol | 2,334 kJ / mol |
| Calor de vaporización | 127,4 kJ / mol | 79,87 kJ / mol |