Este artigo contém uma comparação das principais propriedades térmicas e atômicas de magnésio e potássio, dois elementos químicos comparáveis da tabela periódica. Ele também contém descrições básicas e aplicações de ambos os elementos. Magnésio vs. Potássio.
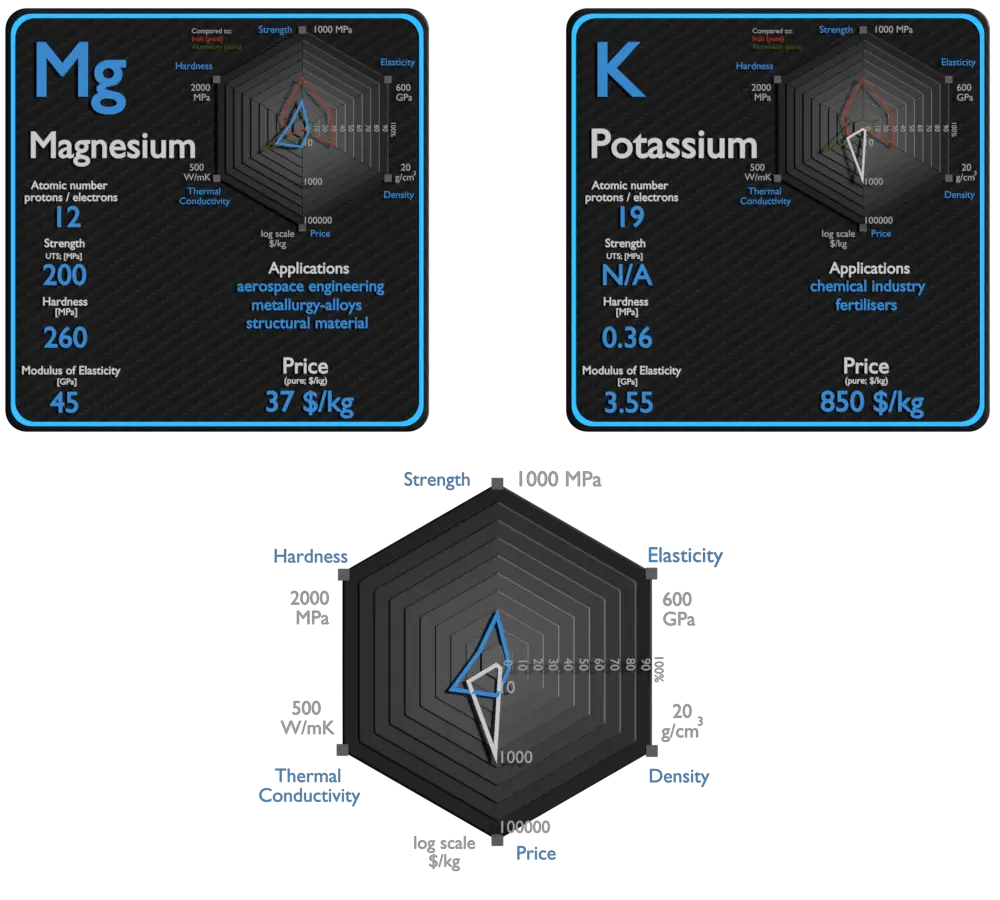
Magnésio e Potássio – Sobre Elementos


Fonte: www.luciteria.com
Magnésio e Potássio – Aplicações
Magnésio
O magnésio é o terceiro metal estrutural mais usado, depois do ferro e do alumínio.[35] As principais aplicações do magnésio são, pela ordem: ligas de alumínio, fundição sob pressão (ligada com zinco), remoção de enxofre na produção de ferro e aço e produção de titânio no processo Kroll. As ligas de magnésio são usadas em uma ampla variedade de aplicações estruturais e não estruturais. As aplicações estruturais incluem equipamentos automotivos, industriais, de manuseio de materiais, comerciais e aeroespaciais. As ligas de magnésio são usadas para peças que operam em altas velocidades e, portanto, devem ser leves para minimizar as forças inerciais. As aplicações comerciais incluem ferramentas portáteis, laptops, malas e escadas, automóveis (por exemplo, volantes e colunas, estruturas de assentos, caixas de transmissão). Magnox (liga), cujo nome é uma abreviação de “magnesium non-oxidizing”, é 99% magnésio e 1% alumínio, e é usado no revestimento de barras de combustível em reatores nucleares magnox.
Potássio
O potássio (K) é um nutriente essencial para o crescimento das plantas. É classificado como macronutriente porque as plantas absorvem grandes quantidades de K durante seu ciclo de vida. Os fertilizantes agrícolas consomem 95% da produção química global de potássio, e cerca de 90% desse potássio é fornecido como KCl. Devido ao seu alto grau de reatividade, o potássio puro raramente é usado em sua forma elementar/metálica. É usado como um poderoso agente redutor em química orgânica. As ligas de potássio/sódio são usadas como meio de troca de calor. O calor no potássio aquece a água e a torna quente o suficiente para ferver. Em seguida, a água é transformada em vapor, que é usado para acionar dispositivos que geram eletricidade.
Magnésio e Potássio – Comparação na Tabela
| Elemento | Magnésio | Potássio |
| Densidade | 1,738 g/cm3 | 0,856 g/cm3 |
| Resistência à tração | 200 MPa | N/D |
| Força de rendimento | N/D | N/D |
| Módulo de elasticidade de Young | 45 GPa | 3,53 GPa |
| Escala de Mohs | 2,5 | 0,4 |
| Dureza Brinell | 260 MPa | 0,36 MPa |
| Dureza Vickers | N/D | N/D |
| Ponto de fusão | 649 °C | 63,25 °C |
| Ponto de ebulição | 1090 °C | 760 °C |
| Condutividade térmica | 156 W/mK | 102,4 W/mK |
| Coeficiente de Expansão Térmica | 24,8 µm/mK | 83 µm/mK |
| Calor específico | 1,02 J/gK | 0,75 J/gK |
| Calor de fusão | 8,954 kJ/mol | 2,334 kJ/mol |
| Calor da vaporização | 127,4 kJ/mol | 79,87 kJ/mol |