Cet article contient une comparaison des principales propriétés thermiques et atomiques du magnésium et du potassium, deux éléments chimiques comparables du tableau périodique. Il contient également des descriptions de base et des applications des deux éléments. Magnésium contre Potassium.
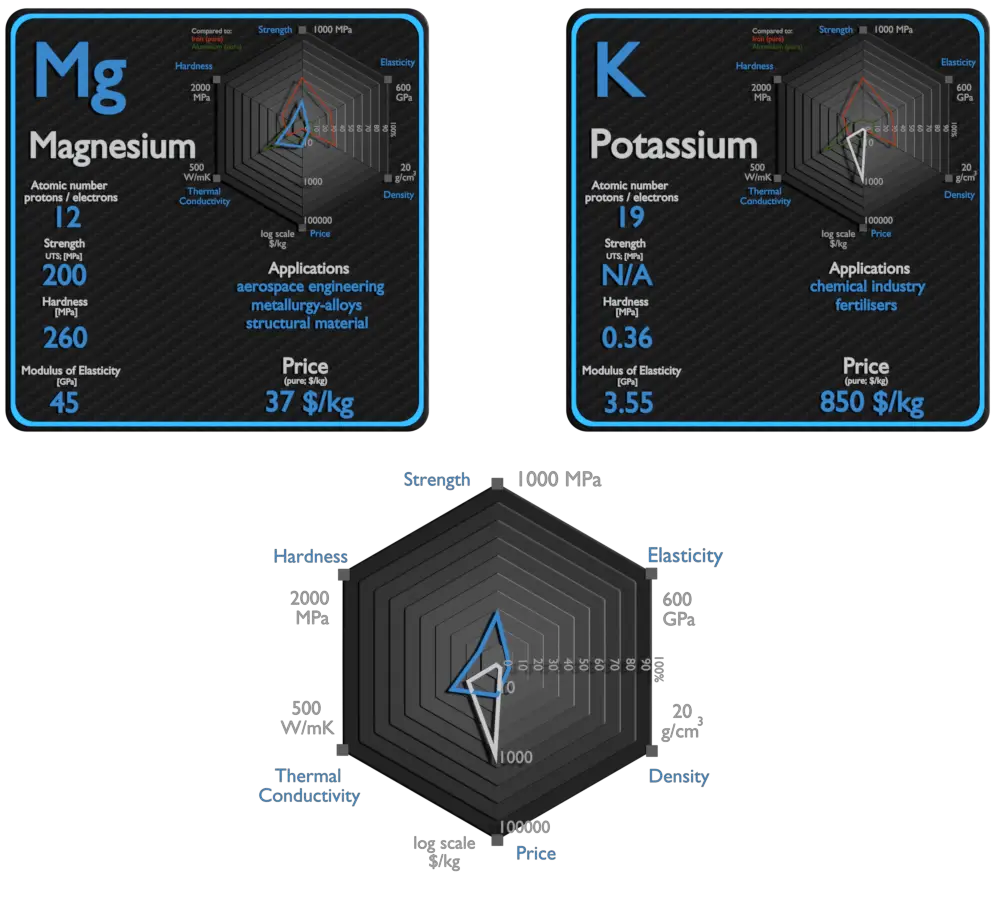
Magnésium et Potassium – À propos des éléments


Source : www.luciteria.com
Magnésium et Potassium – Applications
Magnésium
Le magnésium est le troisième métal de structure le plus couramment utilisé, après le fer et l’aluminium.[35] Les principales applications du magnésium sont, dans l’ordre : les alliages d’aluminium, le moulage sous pression (allié au zinc), l’élimination du soufre dans la production de fer et d’acier, et la production de titane dans le procédé Kroll. Les alliages de magnésium sont utilisés dans une grande variété d’applications structurelles et non structurelles. Les applications structurelles incluent les équipements automobiles, industriels, de manutention, commerciaux et aérospatiaux. Les alliages de magnésium sont utilisés pour les pièces qui fonctionnent à des vitesses élevées et doivent donc être légers pour minimiser les forces d’inertie. Les applications commerciales comprennent les outils portatifs, les ordinateurs portables, les bagages et les échelles, les automobiles (par exemple, les volants et les colonnes, les cadres de siège, les boîtiers de transmission). Magnox (alliage), dont le nom est l’abréviation de « magnésium non oxydant », est composé à 99 % de magnésium et à 1 % d’aluminium, et est utilisé dans le gainage des barres de combustible dans les réacteurs nucléaires magnox.
Potassium
Le potassium (K) est un nutriment essentiel à la croissance des plantes. Il est classé comme macronutriment car les plantes absorbent de grandes quantités de K au cours de leur cycle de vie. Les engrais agricoles consomment 95 % de la production chimique mondiale de potassium, et environ 90 % de ce potassium est fourni sous forme de KCl. En raison de son haut degré de réactivité, le potassium pur est rarement utilisé sous sa forme élémentaire/métallique. Il est utilisé comme puissant agent réducteur en chimie organique. Les alliages Potassium/Sodium sont utilisés comme échangeur de chaleur. La chaleur du potassium réchauffe l’eau et la rend suffisamment chaude pour bouillir. Ensuite, l’eau est transformée en vapeur, qui est utilisée pour faire fonctionner des appareils qui génèrent de l’électricité.
Magnésium et Potassium – Comparaison dans le tableau
| Élément | Magnésium | Potassium |
| Densité | 1,738 g/cm3 | 0,856g/cm3 |
| Résistance à la traction ultime | 200 MPa | N / A |
| Limite d’élasticité | N / A | N / A |
| Module de Young | 45 GPa | 3,53 GPa |
| Échelle de Mohs | 2,5 | 0,4 |
| Dureté Brinell | 260 MPa | 0,36 MPa |
| Dureté Vickers | N / A | N / A |
| Point de fusion | 649°C | 63,25°C |
| Point d’ébullition | 1090°C | 760°C |
| Conductivité thermique | 156 W/mK | 102,4 W/mK |
| Coefficient de dilatation thermique | 24,8 µm/mK | 83 µm/mK |
| Chaleur spécifique | 1,02 J/g·K | 0,75 J/g·K |
| Température de fusion | 8,954 kJ/mol | 2,334 kJ/mole |
| Chaleur de vaporisation | 127,4 kJ/mole | 79,87 kJ/mole |