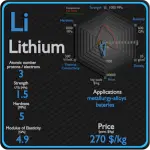
Cet article contient une comparaison des principales propriétés thermiques et atomiques du lithium et du cadmium, deux éléments chimiques comparables du tableau périodique. Il contient également des descriptions de base et des applications des deux éléments. Lithium contre Cadmium.
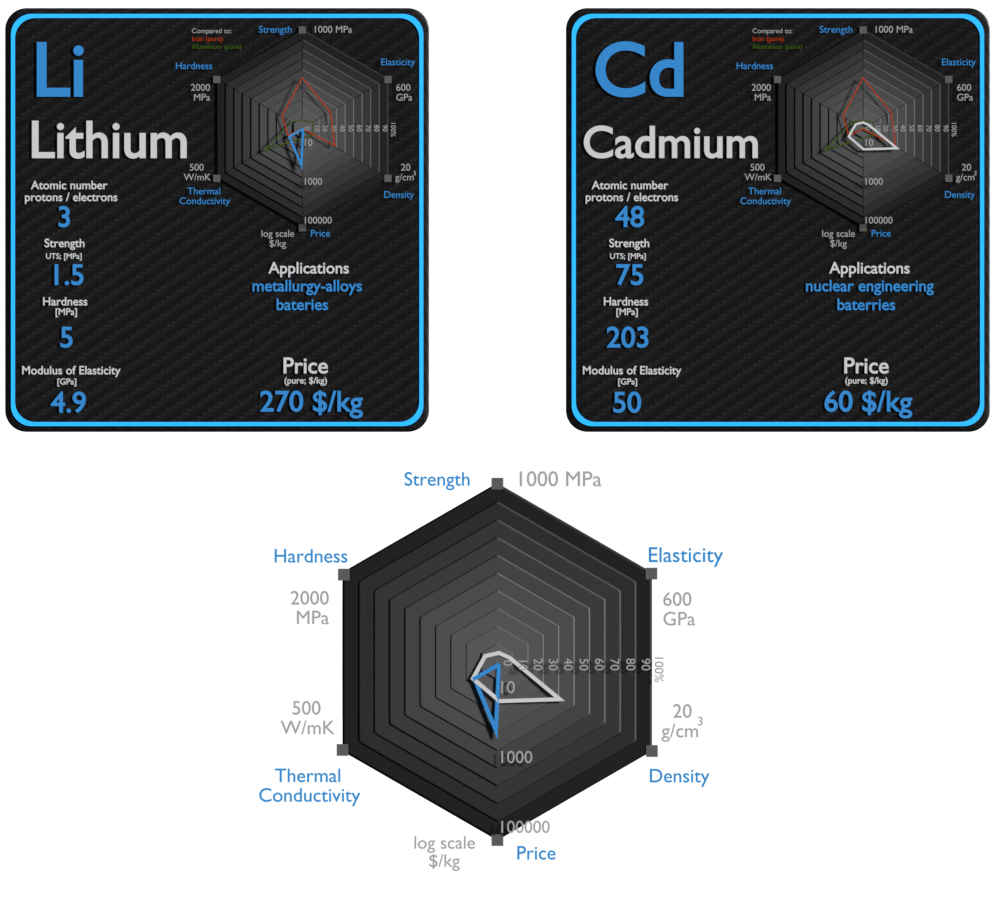
Lithium et Cadmium – À propos des éléments


Source : www.luciteria.com
Lithium et Cadmium – Applications
Lithium
Le lithium a de nombreuses applications, de la graisse lubrifiante, aux ajouts d’alliages notamment pour les alliages d’aluminium et de magnésium, aux émaux pour céramiques, et enfin, les batteries au lithium. En particulier, le lithium joue et continuera de jouer un rôle de plus en plus important dans l’avenir de l’air pur alimenté par batterie. Les batteries au lithium sont largement utilisées dans les appareils électroniques grand public portables et dans les véhicules électriques allant des véhicules de grande taille aux jouets radiocommandés. Le terme « batterie au lithium » fait référence à une famille de différentes chimies lithium-métal, comprenant de nombreux types de cathodes et d’électrolytes, mais tous avec du lithium métallique comme anode.
Cadmium
Le cadmium est principalement consommé pour la production de batteries rechargeables au nickel-cadmium. En 2009, 86 % du cadmium était utilisé dans les piles, principalement dans les piles rechargeables au nickel-cadmium. Les autres utilisations finales comprennent les pigments, les revêtements et le placage, et comme stabilisants pour les plastiques. La fabrication de cellules solaires pourrait devenir un autre marché important pour le cadmium à l’avenir. Dans l’industrie nucléaire, le cadmium est couramment utilisé comme absorbeur de neutrons thermiques en raison de la section efficace d’absorption des neutrons très élevée de 113Cd. Le 113Cd a une section efficace d’absorption spécifique.
Lithium et Cadmium – Comparaison dans le tableau
| Élément | Lithium | Cadmium |
| Densité | 0,535 g/cm3 | 8,65 g/cm3 |
| Résistance à la traction ultime | 1,5 MPa | 75 MPa |
| Limite d’élasticité | N / A | N / A |
| Module de Young | 4,9 GPa | 50 GPa |
| Échelle de Mohs | 0,6 | 2 |
| Dureté Brinell | 5 MPa | 203 MPa |
| Dureté Vickers | N / A | N / A |
| Point de fusion | 180,5 °C | 321,07 °C |
| Point d’ébullition | 1342 °C | 767 °C |
| Conductivité thermique | 85 W/mK | 97 W/mK |
| Coefficient de dilatation thermique | 46 µm/mK | 30,8 µm/mK |
| Chaleur spécifique | 3,6 J/g·K | 0,23 J/g·K |
| Température de fusion | 3 kJ/mol | 6,192 kJ/mol |
| Chaleur de vaporisation | 145,92 kJ/mol | 99,57 kJ/mol |