Cet article contient une comparaison des principales propriétés thermiques et atomiques du lithium et du cobalt, deux éléments chimiques comparables du tableau périodique. Il contient également des descriptions de base et des applications des deux éléments. Lithium contre Cobalt.
Lithium et Cobalt – À propos des éléments


Source : www.luciteria.com
Lithium et Cobalt – Applications
Lithium
Le lithium a de nombreuses applications, de la graisse lubrifiante, aux ajouts d’alliages notamment pour les alliages d’aluminium et de magnésium, aux émaux pour céramiques, et enfin, les batteries au lithium. En particulier, le lithium joue et continuera de jouer un rôle de plus en plus important dans l’avenir de l’air pur alimenté par batterie. Les batteries au lithium sont largement utilisées dans les appareils électroniques grand public portables et dans les véhicules électriques allant des véhicules de grande taille aux jouets radiocommandés. Le terme « batterie au lithium » fait référence à une famille de différentes chimies lithium-métal, comprenant de nombreux types de cathodes et d’électrolytes, mais tous avec du lithium métallique comme anode.
Cobalt
Le cobalt a été utilisé dans de nombreuses applications industrielles, commerciales et militaires. Le cobalt est principalement utilisé dans les batteries lithium-ion et dans la fabrication d’alliages magnétiques, résistants à l’usure et à haute résistance. Superalliages à base de cobalt. Cette classe d’alliages est relativement nouvelle. En 2006, Sato et al. découvert une nouvelle phase dans le système Co–Al–W. Contrairement aux autres superalliages, les alliages à base de cobalt se caractérisent par une matrice austénitique renforcée en solution solide (fcc) dans laquelle une faible quantité de carbure est distribuée. Bien qu’ils ne soient pas utilisés commercialement dans la mesure des superalliages à base de Ni, les éléments d’alliage trouvés dans les alliages à base de Co de recherche sont C, Cr, W, Ni, Ti, Al, Ir et Ta. Ils possèdent une meilleure soudabilité et une meilleure résistance à la fatigue thermique par rapport à l’alliage à base de nickel. En outre, ils ont une excellente résistance à la corrosion à haute température (980-1100 °C) en raison de leur teneur en chrome plus élevée. Plusieurs composés du cobalt sont des catalyseurs d’oxydation. Les catalyseurs typiques sont les carboxylates de cobalt (appelés savons de cobalt). Ils sont également utilisés dans les peintures, les vernis et les encres en tant qu' »agents siccatifs » grâce à l’oxydation des huiles siccatives.
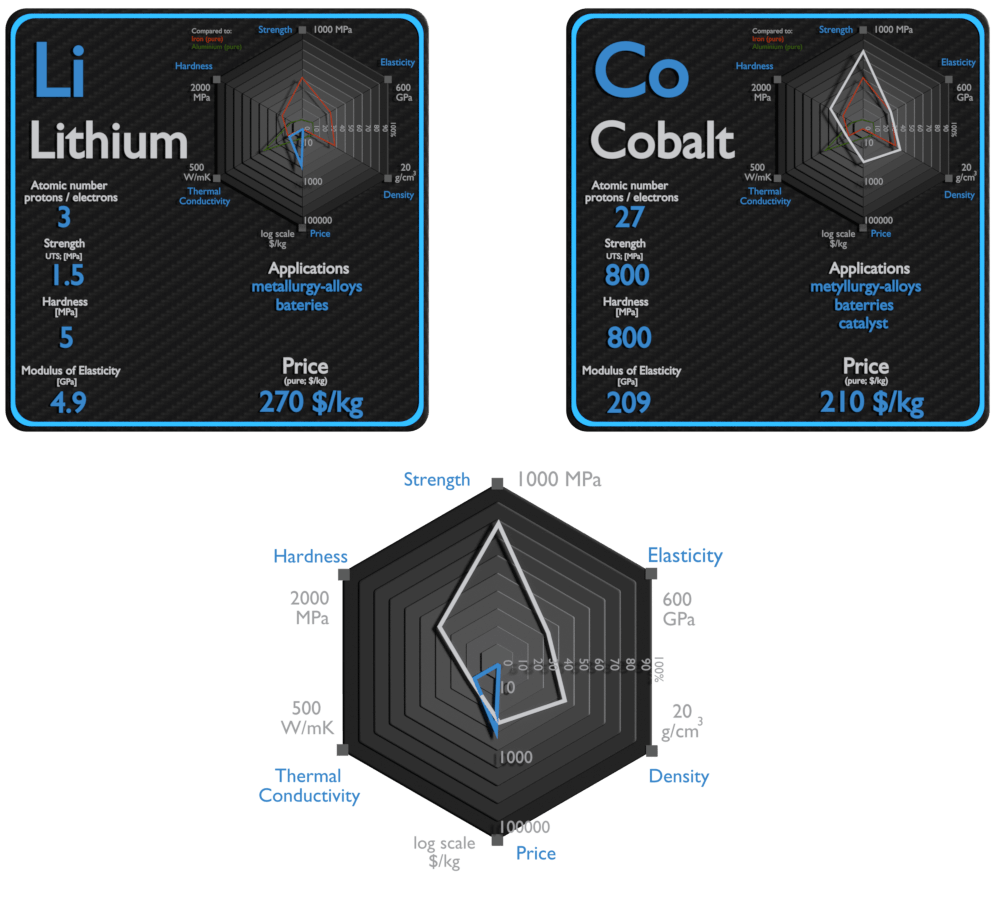
Lithium et Cobalt – Comparaison dans le tableau
| Élément | Lithium | Cobalt |
| Densité | 0,535 g/cm3 | 8,9 g/cm3 |
| Résistance à la traction ultime | 1,5 MPa | 800 MPa |
| Limite d’élasticité | N / A | 220 MPa |
| Module de Young | 4,9 GPa | 209 GPa |
| Échelle de Mohs | 0,6 | 5 |
| Dureté Brinell | 5 MPa | 800 MPa |
| Dureté Vickers | N / A | 1040 MPa |
| Point de fusion | 180,5 °C | 1495 °C |
| Point d’ébullition | 1342 °C | 2927 °C |
| Conductivité thermique | 85 W/mK | 100 W/mK |
| Coefficient de dilatation thermique | 46 µm/mK | 13 µm/mK |
| Chaleur spécifique | 3,6 J/g·K | 0,42 J/g·K |
| Température de fusion | 3 kJ/mol | 16,19 kJ/mol |
| Chaleur de vaporisation | 145,92 kJ/mol | 376,5 kJ/mol |