O disprósio é um elemento de terras raras com brilho prateado metálico. O disprósio é utilizado por sua alta seção transversal de absorção de nêutrons térmicos na fabricação de hastes de controle em reatores nucleares, por sua alta suscetibilidade magnética em aplicações de armazenamento de dados.
Resumo
| Elemento | Disprósio |
| Número atômico | 66 |
| Massa atômica [amu] | 162,5 |
| Massa atômica [pm] | 178 |
| Densidade em STP [g/cm3] | 8,551 |
| Número de prótons | 66 |
| Número de nêutrons (isótopos típicos) | 156-164 |
| Número de elétrons | 66 |
| Configuração eletrônica | [Veículo] 4f10 6s2 |
| Estados de oxidação | +3 |
| Afinidade eletrônica [kJ/mol] | 50 |
| Eletronegatividade [escala de Pauling] | 1,22 |
| Primeira energia de ionização [eV] | 5,9389 |
Número atômico – prótons, elétrons e nêutrons em Disprósio
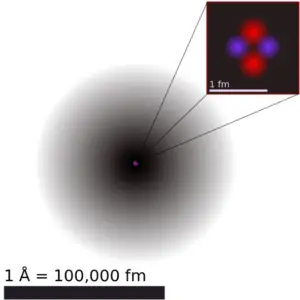
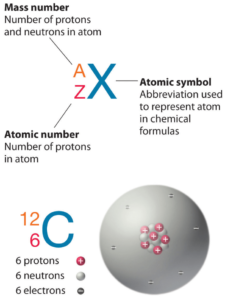 O disprósio é um elemento químico com número atômico 66, o que significa que há 66 prótons em seu núcleo. O número total de prótons no núcleo é chamado de número atômico do átomo e recebe o símbolo Z. A carga elétrica total do núcleo é, portanto, +Ze, onde e (carga elementar) é igual a 1,602 x 10-19 coulombs.
O disprósio é um elemento químico com número atômico 66, o que significa que há 66 prótons em seu núcleo. O número total de prótons no núcleo é chamado de número atômico do átomo e recebe o símbolo Z. A carga elétrica total do núcleo é, portanto, +Ze, onde e (carga elementar) é igual a 1,602 x 10-19 coulombs.
O número total de nêutrons no núcleo de um átomo é chamado de número de nêutrons do átomo e recebe o símbolo N. O número de nêutrons mais o número atômico é igual ao número de massa atômica: N+Z=A. A diferença entre o número de nêutrons e o número atômico é conhecido como excesso de nêutrons: D = N – Z = A – 2Z.
Para elementos estáveis, geralmente há uma variedade de isótopos estáveis. Isótopos são nuclídeos que têm o mesmo número atômico e, portanto, são o mesmo elemento, mas diferem no número de nêutrons. Os números de massa de isótopos típicos de disprósio são 156-164.
Massa Atômica de Disprósio
A massa atômica do disprósio é 162,5 u.
A massa atômica é a massa de um átomo. A massa atômica ou massa isotópica relativa refere-se à massa de uma única partícula e, portanto, está ligada a um certo isótopo específico de um elemento. A massa atômica é transportada pelo núcleo atômico, que ocupa apenas cerca de 10-12 do volume total do átomo ou menos, mas contém toda a carga positiva e pelo menos 99,95% da massa total do átomo. Observe que cada elemento pode conter mais isótopos, portanto, essa massa atômica resultante é calculada a partir de isótopos de ocorrência natural e sua abundância.
Raio Atômico do Disprósio
O raio atômico do átomo de disprósio é 178pm (raio covalente).
Deve-se notar que os átomos não possuem um limite externo bem definido. O raio atômico de um elemento químico é uma medida da distância até a qual a nuvem de elétrons se estende do núcleo. No entanto, isso pressupõe que o átomo apresente uma forma esférica, que só é obedecida para átomos no vácuo ou no espaço livre. Portanto, existem várias definições não equivalentes de raio atômico.
Elétrons e configuração eletrônica
O número de elétrons em um átomo eletricamente neutro é o mesmo que o número de prótons no núcleo. Portanto, o número de elétrons no átomo neutro de Disprósio é 66. Cada elétron é influenciado pelos campos elétricos produzidos pela carga nuclear positiva e os demais (Z – 1) elétrons negativos no átomo.
Uma vez que o número de elétrons e seu arranjo são responsáveis pelo comportamento químico dos átomos, o número atômico identifica os vários elementos químicos. A configuração desses elétrons segue os princípios da mecânica quântica. O número de elétrons nas camadas eletrônicas de cada elemento, particularmente a camada de valência mais externa, é o principal fator para determinar seu comportamento de ligação química. Na tabela periódica, os elementos são listados em ordem crescente de número atômico Z.
A configuração eletrônica do disprósio é [Xe] 4f10 6s2.
Os estados de oxidação possíveis são +3.
Densidade de Disprósio
A densidade do disprósio é de 8,551g/cm3 .
As densidades típicas de várias substâncias estão à pressão atmosférica.
A densidade é definida como a massa por unidade de volume. É uma propriedade intensiva, que é matematicamente definida como massa dividida pelo volume:
ρ = m/V
Afinidade Eletrônica – Disprósio
A afinidade eletrônica do disprósio é de 50 kJ/mol.
Em química e física atômica, a afinidade eletrônica de um átomo ou molécula é definida como:
a mudança na energia (em kJ/mol) de um átomo ou molécula neutra (na fase gasosa) quando um elétron é adicionado ao átomo para formar um íon negativo.
X + e – → X – + energia Afinidade = – ∆H
Em outras palavras, pode ser expresso como a probabilidade do átomo neutro ganhar um elétron. Observe que as energias de ionização medem a tendência de um átomo neutro de resistir à perda de elétrons. As afinidades eletrônicas são mais difíceis de medir do que as energias de ionização.
Eletronegatividade do Disprósio
A eletronegatividade do disprósio é 1,22.
A eletronegatividade, símbolo χ, é uma propriedade química que descreve a tendência de um átomo de atrair elétrons para este átomo. Para isso, uma grandeza adimensional da escala de Pauling, símbolo χ, é a mais utilizada.
A eletronegatividade do disprósio é: χ = 1,22
Primeira energia de ionização do Disprósio
A primeira energia de ionização do disprósio é 5,9389 eV.
A energia de ionização, também chamada de potencial de ionização, é a energia necessária para remover um elétron do átomo neutro.
X + energia → X + + e −
onde X é qualquer átomo ou molécula capaz de ser ionizado, X+ é aquele átomo ou molécula com um elétron removido (íon positivo) e e− é o elétron removido.
Um átomo de disprósio, por exemplo, requer a seguinte energia de ionização para remover o elétron mais externo.
Dy + IE → Dy + + e − IE = 5,9389 eV
Fonte: www.luciteria.com