Este artigo contém uma comparação das principais propriedades térmicas e atômicas do titânio e do urânio, dois elementos químicos comparáveis da tabela periódica. Ele também contém descrições básicas e aplicações de ambos os elementos. Titânio vs. Urânio.
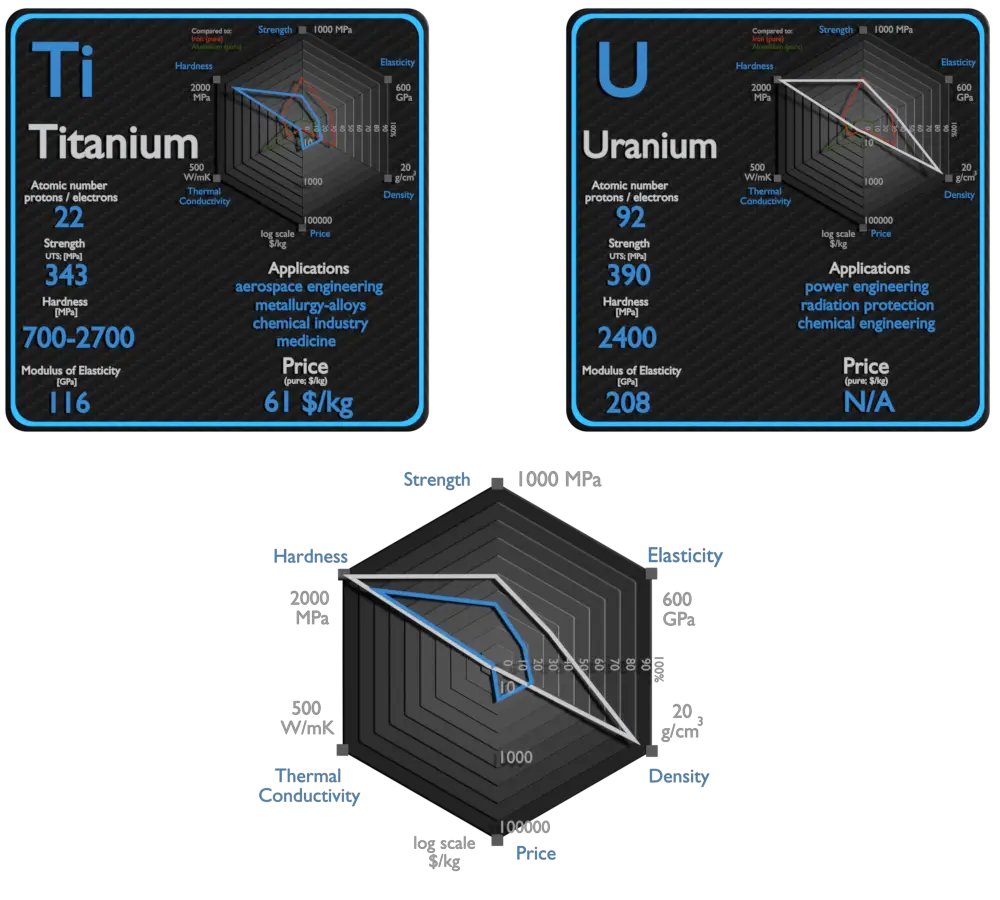
Titânio e Urânio – Sobre Elementos


Fonte: www.luciteria.com
Titânio e Urânio – Aplicações
Titânio
As duas propriedades mais úteis do metal são a resistência à corrosão e a relação resistência-densidade, a mais alta de qualquer elemento metálico. A resistência à corrosão das ligas de titânio em temperaturas normais é excepcionalmente alta. Essas propriedades determinam a aplicação do titânio e suas ligas. A primeira aplicação de produção de titânio foi em 1952, para as naceles e firewalls do avião Douglas DC-7. Alta resistência específica, boa resistência à fadiga e vida útil à fluência e boa tenacidade à fratura são características que tornam o titânio um metal preferido para aplicações aeroespaciais. As aplicações aeroespaciais, incluindo o uso em componentes estruturais (fuselagem) e motores a jato, ainda representam a maior parte do uso de ligas de titânio. Na aeronave supersônica SR-71, o titânio foi usado em 85% da estrutura. Devido à inércia muito alta,
Urânio
O principal uso de urânio no setor civil é para abastecer usinas nucleares. Um quilograma de urânio-235 pode teoricamente produzir cerca de 20 terajoules de energia, assumindo fissão completa; tanta energia quanto 1,5 milhão de quilogramas (1.500 toneladas) de carvão. O reator típico pode conter cerca de 100 toneladas de urânio enriquecido (ou seja, cerca de 113 toneladas de dióxido de urânio). Este combustível é carregado, por exemplo, em 157 conjuntos de combustível compostos por mais de 45.000 barras de combustível. Um conjunto de combustível comum contém energia para aproximadamente 4 anos de operação em potência máxima. O combustível removido (combustível nuclear gasto) ainda contém cerca de 96% de material reutilizável (deve ser removido devido à diminuição do kinf de um conjunto). Antes (e, ocasionalmente, depois) da descoberta da radioatividade, o urânio era usado principalmente em pequenas quantidades para vidro amarelo e esmaltes de cerâmica, como vidro de urânio. O urânio também é usado pelos militares para alimentar submarinos nucleares e em armas nucleares. Devido à sua alta densidade, este material é encontrado em sistemas de orientação inercial e em bússolas giroscópicas.[10] O urânio empobrecido é preferido em relação aos metais igualmente densos devido à sua capacidade de ser facilmente usinado e fundido, bem como seu custo relativamente baixo. O principal risco de exposição ao urânio empobrecido é o envenenamento químico por óxido de urânio, em vez de radioatividade (o urânio é apenas um emissor alfa fraco). O urânio empobrecido é o urânio que tem muito menos urânio-235 do que o urânio natural. É consideravelmente menos radioativo que o urânio natural. É um metal denso que pode ser usado como lastro para navios e contrapesos para aeronaves. Também é usado em munições e armaduras. O urânio empobrecido também pode ser usado para proteger a radiação. O urânio empobrecido é muito mais eficaz devido ao seu Z mais alto. O urânio empobrecido é usado para blindagem em fontes portáteis de raios gama. O urânio é usado em aços rápidos como agente de liga para melhorar a resistência e a tenacidade. O trióxido de urânio (também chamado de óxido urânico) com fórmula UO3, é um pó amarelo alaranjado e é usado como pigmento para cerâmica. Em copos produz um belo “vidro de urânio” amarelo-esverdeado.
Titânio e Urânio – Comparação na Tabela
| Elemento | Titânio | Urânio |
| Densidade | 4,507 g/cm3 | 19,05 g/cm3 |
| Resistência à tração | 434 MPa, 293 MPa (puro) | 390 MPa |
| Força de rendimento | 380 MPa | 190 MPa |
| Módulo de elasticidade de Young | 116 GPa | 208 GPa |
| Escala de Mohs | 6 | 6 |
| Dureza Brinell | 700 – 2700 MPa | 2400 MPa |
| Dureza Vickers | 800 – 3400 MPa | 1960 MPa |
| Ponto de fusão | 1668 °C | 1132 °C |
| Ponto de ebulição | 3287 °C | 4131 °C |
| Condutividade térmica | 21,9 W/mK | 27 W/mK |
| Coeficiente de Expansão Térmica | 8,6 µm/mK | 13,9 µm/mK |
| Calor específico | 0,52 J/gK | 0,12 J/gK |
| Calor de fusão | 15,45 kJ/mol | 8,52 kJ/mol |
| Calor da vaporização | 421 kJ/mol | 417 kJ/mol |