Cet article contient une comparaison des principales propriétés thermiques et atomiques du lithium et du sodium, deux éléments chimiques comparables du tableau périodique. Il contient également des descriptions de base et des applications des deux éléments. Lithium contre Sodium.
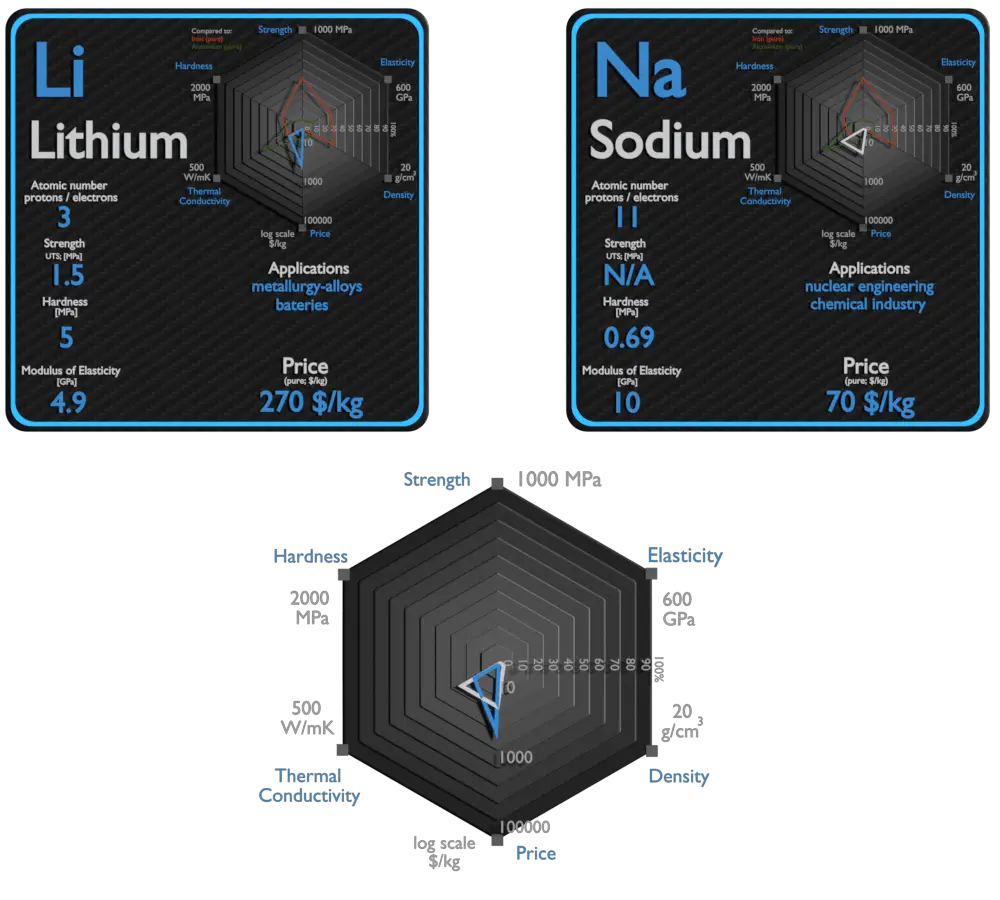
Lithium et Sodium – À propos des éléments


Source : www.luciteria.com
Lithium et Sodium – Applications
Lithium
Le lithium a de nombreuses applications, de la graisse lubrifiante, aux ajouts d’alliages notamment pour les alliages d’aluminium et de magnésium, aux émaux pour céramiques, et enfin, les batteries au lithium. En particulier, le lithium joue et continuera de jouer un rôle de plus en plus important dans l’avenir de l’air pur alimenté par batterie. Les batteries au lithium sont largement utilisées dans les appareils électroniques grand public portables et dans les véhicules électriques allant des véhicules de grande taille aux jouets radiocommandés. Le terme « batterie au lithium » fait référence à une famille de différentes chimies lithium-métal, comprenant de nombreux types de cathodes et d’électrolytes, mais tous avec du lithium métallique comme anode.
Sodium
Le sodium métallique est principalement utilisé pour la production de borohydrure de sodium, d’azoture de sodium, d’indigo et de triphénylphosphine. Une utilisation autrefois courante était la fabrication de tétraéthylplomb et de titane métallique; en raison de l’abandon du TEL et des nouvelles méthodes de production de titane. Un courant électrique et de la vapeur de sodium se combinent pour former une lueur jaunâtre. Ce principe est utilisé pour la fabrication des lampes à vapeur de sodium. Le sodium est parfois utilisé comme agent d’échange de chaleur dans les centrales nucléaires. Le sodium liquide est scellé dans des tuyaux entourant le cœur du réacteur. La chaleur générée est absorbée par le sodium et forcée à travers les tuyaux dans un échangeur de chaleur qui peut être utilisé pour générer de l’électricité.
Lithium et Sodium – Comparaison dans le tableau
| Élément | Lithium | Sodium |
| Densité | 0,535g/cm3 | 0,968g/cm3 |
| Résistance à la traction ultime | 1,5 MPa | N / A |
| Limite d’élasticité | N / A | N / A |
| Module de Young | 4,9 GPa | 10 GPa |
| Échelle de Mohs | 0,6 | 0,4 |
| Dureté Brinell | 5 MPa | 0,69 MPa |
| Dureté Vickers | N / A | N / A |
| Point de fusion | 180,5 °C | 97,8 °C |
| Point d’ébullition | 1342° C | 883 °C |
| Conductivité thermique | 85W/mK | 141W/mK |
| Coefficient de dilatation thermique | 46 µm/mK | 71 µm/mK |
| Chaleur spécifique | 3,6 J/g·K | 1,23 J/g·K |
| Température de fusion | 3 kJ/mol | 2,59 kJ/mol |
| Chaleur de vaporisation | 145,92 kJ/mol | 96,96 kJ/mol |