Este artículo contiene una comparación de las propiedades térmicas y atómicas clave del litio y el cobalto, dos elementos químicos comparables de la tabla periódica. También contiene descripciones básicas y aplicaciones de ambos elementos. Litio vs Cobalto.
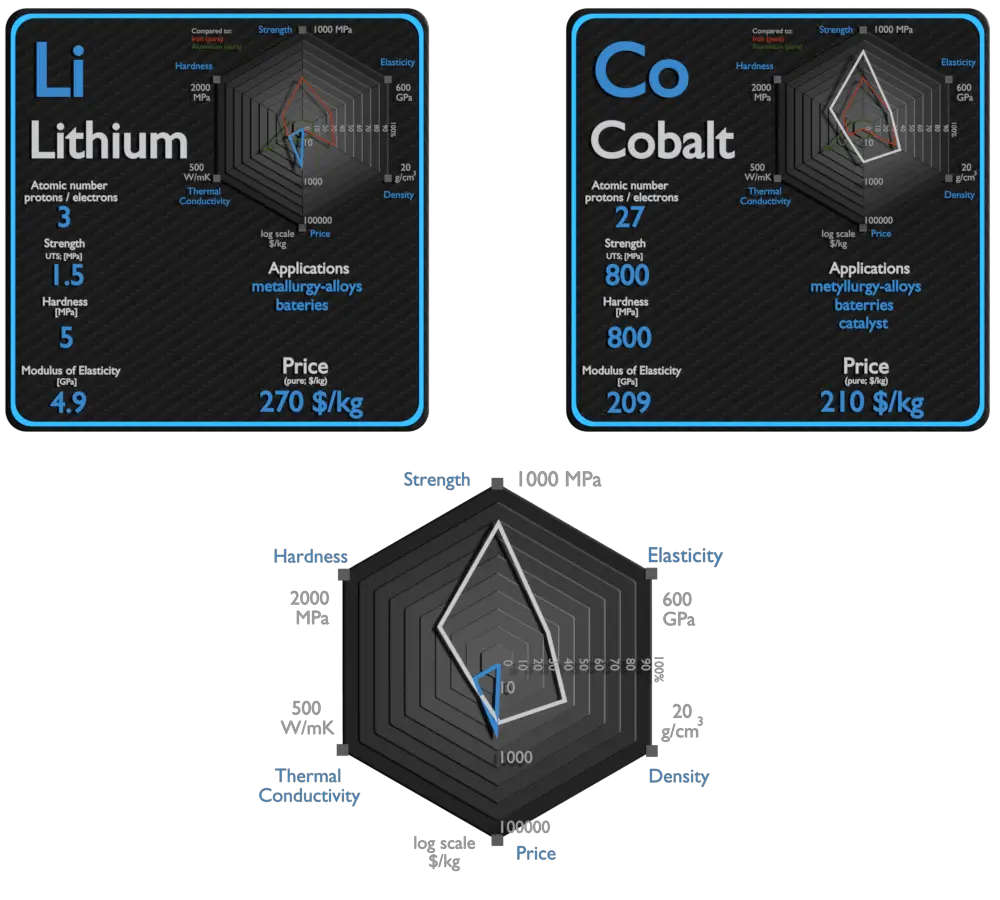
Litio y Cobalto: acerca de los elementos


Fuente: www.luciteria.com
Litio y Cobalto: aplicaciones
Litio
El litio tiene muchas aplicaciones, desde grasas lubricantes, adiciones de aleación, en particular para aleaciones de aluminio y magnesio, hasta esmaltes para cerámica y, finalmente, baterías de litio. En particular, el litio es y seguirá desempeñando un papel cada vez más importante en el futuro del aire limpio alimentado por baterías. Las baterías de litio se utilizan ampliamente en dispositivos electrónicos portátiles de consumo y en vehículos eléctricos que van desde vehículos de tamaño completo hasta juguetes controlados por radio. El término «batería de litio» se refiere a una familia de diferentes químicas de litio-metal, que comprende muchos tipos de cátodos y electrolitos, pero todos con litio metálico como ánodo.
Cobalto
El cobalto se ha utilizado en muchas aplicaciones industriales, comerciales y militares. El cobalto se utiliza principalmente en baterías de iones de litio y en la fabricación de aleaciones magnéticas, resistentes al desgaste y de alta resistencia. Superaleaciones a base de cobalto. Esta clase de aleaciones es relativamente nueva. En 2006, Sato et al. descubrió una nueva fase en el sistema Co – Al – W. A diferencia de otras superaleaciones, las aleaciones a base de cobalto se caracterizan por una matriz austenítica reforzada con solución sólida (fcc) en la que se distribuye una pequeña cantidad de carburo. Aunque no se utilizan comercialmente en la medida de las superaleaciones a base de Ni, los elementos de aleación que se encuentran en las aleaciones a base de Co para la investigación son C, Cr, W, Ni, Ti, Al, Ir y Ta. Poseen mejor soldabilidad y resistencia a la fatiga térmica en comparación con la aleación a base de níquel. Es más, tienen una excelente resistencia a la corrosión a altas temperaturas (980-1100 °C) debido a su mayor contenido de cromo. Varios compuestos de cobalto son catalizadores de oxidación. Los catalizadores típicos son los carboxilatos de cobalto (conocidos como jabones de cobalto). También se utilizan en pinturas, barnices y tintas como «agentes secantes» a través de la oxidación de los aceites secantes.
Litio y Cobalto: comparación en la tabla
| Elemento | Litio | Cobalto |
| Densidad | 0,535 g/cm3 | 8,9 g/cm3 |
| Resistencia a la tracción | 1,5 MPa | 800 MPa |
| Límite de elastacidad | N / A | 220 MPa |
| Módulo de Young | 4,9 GPa | 209 GPa |
| Escala de Mohs | 0,6 | 5 |
| Dureza Brinell | 5 MPa | 800 MPa |
| Dureza Vickers | N / A | 1040 MPa |
| Punto de fusion | 180,5 °C | 1495 °C |
| Punto de ebullición | 1342 °C | 2927 °C |
| Conductividad térmica | 85 W/mK | 100 W/mK |
| Coeficiente de expansión térmica | 46 µm/mK | 13 µm/mK |
| Calor especifico | 3,6 J/g K | 0,42 J/g K |
| Calor de fusión | 3 kJ/mol | 16,19 kJ/mol |
| Calor de vaporización | 145,92 kJ/mol | 376,5 kJ/mol |