Este artigo contém uma comparação das principais propriedades térmicas e atômicas do lítio e do cobalto, dois elementos químicos comparáveis da tabela periódica. Ele também contém descrições básicas e aplicações de ambos os elementos. Lítio vs. Cobalto.
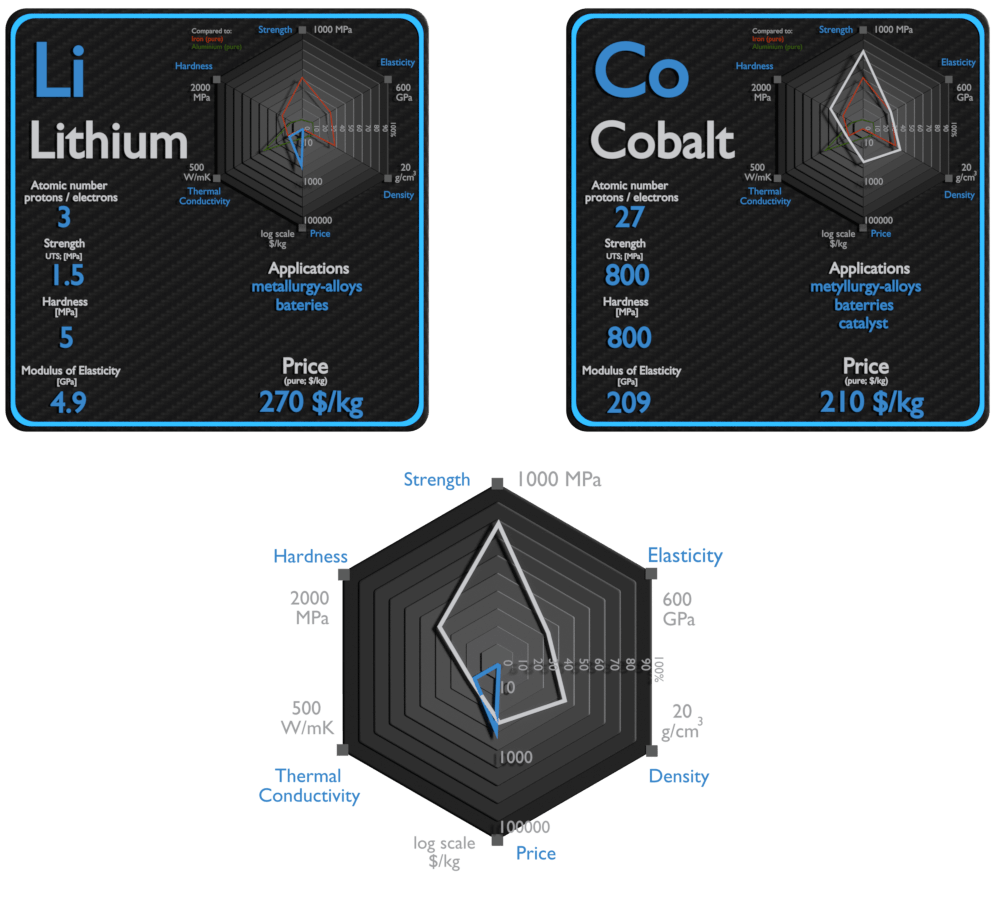
Lítio e Cobalto – Sobre Elementos


Fonte: www.luciteria.com
O lítio tem muitas aplicações, desde graxa lubrificante, adições de ligas em particular para ligas de alumínio e magnésio, até esmaltes para cerâmica e, finalmente, baterias de lítio. Em particular, o lítio é e continuará a desempenhar um papel cada vez mais importante no futuro do ar limpo movido a bateria. As baterias de lítio são amplamente utilizadas em dispositivos eletrônicos de consumo portáteis e em veículos elétricos, desde veículos de tamanho normal até brinquedos controlados por rádio. O termo “bateria de lítio” refere-se a uma família de diferentes composições químicas de lítio-metal, compreendendo muitos tipos de cátodos e eletrólitos, mas todos com lítio metálico como ânodo. O cobalto tem sido usado em muitas aplicações industriais, comerciais e militares. O cobalto é usado principalmente em baterias de íons de lítio e na fabricação de ligas magnéticas, resistentes ao desgaste e de alta resistência. Superligas à base de cobalto. Esta classe de ligas é relativamente nova. Em 2006, Sato et al. descobriu uma nova fase no sistema Co-Al-W. Ao contrário de outras superligas, as ligas à base de cobalto são caracterizadas por uma matriz austenítica reforçada por solução sólida (FCC) na qual uma pequena quantidade de carboneto é distribuída. Embora não sejam usados comercialmente na extensão de superligas à base de Ni, os elementos de liga encontrados em pesquisas de ligas à base de Co são C, Cr, W, Ni, Ti, Al, Ir e Ta. Eles possuem melhor soldabilidade e resistência à fadiga térmica em comparação com a liga à base de níquel. Além disso, eles têm excelente resistência à corrosão em altas temperaturas (980-1100 °C) devido ao seu alto teor de cromo. Vários compostos de cobalto são catalisadores de oxidação. Os catalisadores típicos são os carboxilatos de cobalto (conhecidos como sabões de cobalto). Eles também são usados em tintas, vernizes e tintas como “agentes de secagem” através da oxidação de óleos de secagem.Lítio e Cobalto – Aplicações
Lítio
Cobalto
Lítio e Cobalto – Comparação na Tabela
Elemento
Lítio
Cobalto
Densidade
0,535 g/cm3
8,9 g/cm3
Resistência à tração
1,5 MPa
800 MPa
Força de Rendimento
N/D
220 MPa
Módulo de elasticidade de Young
4,9 GPa
209 GPa
Escala de Mohs
0,6
5
Dureza Brinell
5 MPa
800 MPa
Dureza Vickers
N/D
1040 MPa
Ponto de fusão
180,5 °C
1495 °C
Ponto de ebulição
1342 °C
2927 °C
Condutividade térmica
85 W/mK
100 W/mK
Coeficiente de Expansão Térmica
46 µm/mK
13 µm/mK
Calor específico
3,6 J/gK
0,42 J/gK
Calor de fusão
3 kJ/mol
16,19 kJ/mol
Calor da vaporização
145,92 kJ/mol
376,5 kJ/mol