L’astatine est l’élément naturel le plus rare de la croûte terrestre. Il se produit sur Terre en tant que produit de désintégration de divers éléments plus lourds. Les propriétés globales de l’astatine ne sont pas connues avec certitude.
Protons et neutrons dans l’Astatine
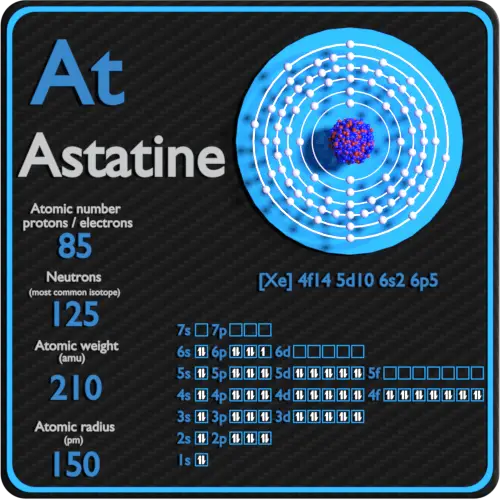
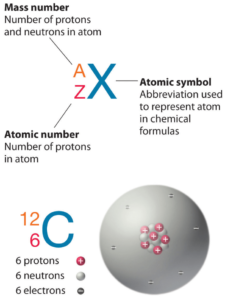 L’astatine est un élément chimique de numéro atomique 85, ce qui signifie qu’il y a 85 protons dans son noyau. Le nombre total de protons dans le noyau est appelé le numéro atomique de l’atome et reçoit le symbole Z. La charge électrique totale du noyau est donc +Ze, où e (charge élémentaire) vaut 1 602 x 10-19 coulombs.
L’astatine est un élément chimique de numéro atomique 85, ce qui signifie qu’il y a 85 protons dans son noyau. Le nombre total de protons dans le noyau est appelé le numéro atomique de l’atome et reçoit le symbole Z. La charge électrique totale du noyau est donc +Ze, où e (charge élémentaire) vaut 1 602 x 10-19 coulombs.
Le nombre total de neutrons dans le noyau d’un atome est appelé le nombre de neutrons de l’atome et reçoit le symbole N. Le nombre de neutrons plus le numéro atomique est égal au nombre de masse atomique: N+Z=A . La différence entre le nombre de neutrons et le numéro atomique est appelée excès de neutrons: D = N – Z = A – 2Z.
Pour les éléments stables, il existe généralement une variété d’isotopes stables. Les isotopes sont des nucléides qui ont le même numéro atomique et sont donc le même élément, mais diffèrent par le nombre de neutrons. Les nombres de masse des isotopes typiques de l’astatine sont de 210.
Principaux isotopes de l’Astatine
L’astatine n’existe pas sous forme naturelle.
Isotopes instables typiques
| Isotope | Demi-vie | Mode de décomposition | Produit |
| 209At | 5h 41 | désintégration bêta plus ou désintégration alpha | 209Po ou 205Bi |
| 210At | 8,1 h | désintégration bêta plus ou désintégration alpha | 210Po ou 206Bi |
| 211At | 7h 21 | capture d’électrons ou désintégration alpha | 211Po ou 207Bi |
[/ su_panel]
[/ su_shadow]
Électrons et configuration électronique
Le nombre d’électrons dans un atome électriquement neutre est le même que le nombre de protons dans le noyau. Par conséquent, le nombre d’électrons dans l’atome neutre d’ Astatine est de 85. Chaque électron est influencé par les champs électriques produits par la charge nucléaire positive et les autres (Z – 1) électrons négatifs de l’atome.
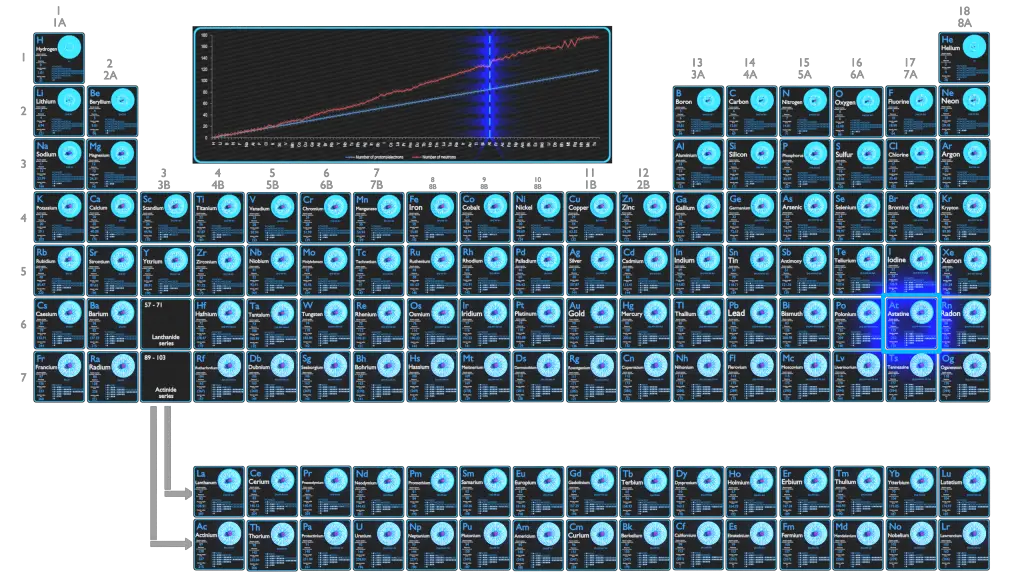
Le nombre d’électrons et leur disposition étant responsables du comportement chimique des atomes, le numéro atomique identifie les différents éléments chimiques. La configuration de ces électrons découle des principes de la mécanique quantique. Le nombre d’électrons dans les couches d’électrons de chaque élément, en particulier la couche de valence la plus externe, est le principal facteur déterminant son comportement de liaison chimique. Dans le tableau périodique, les éléments sont classés par ordre croissant de numéro atomique Z.
La configuration électronique de l’astatine est [Hg] 6p5.
Les états d’oxydation possibles sont.
Résumé
| Élément | Astatine |
| Nombre de protons | 85 |
| Nombre de neutrons (isotopes typiques) | 210 |
| Nombre d’électrons | 85 |
| Configuration électronique | [Hg] 6p5 |
| États d’oxydation |
Source : www.luciteria.com