El carbono no es metálico y tetravalente, lo que hace que cuatro electrones estén disponibles para formar enlaces químicos covalentes. El carbono es uno de los pocos elementos conocidos desde la antigüedad.
El principal uso económico del carbono, además de los alimentos y la madera, es en forma de hidrocarburos, sobre todo el gas metano de combustibles fósiles y el petróleo crudo (petróleo). El grafito y los diamantes son dos alótropos importantes del carbono que tienen amplias aplicaciones. Los usos del carbono y sus compuestos son extremadamente variados.
El grafito, el diamante y otras formas de carbono se obtienen directamente de las minas.
Protones y neutrones en Carbono
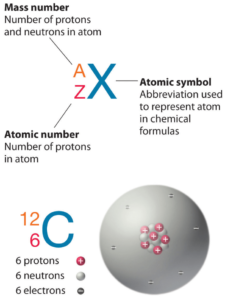 El carbono es un elemento químico con número atómico 6, lo que significa que hay 6 protones en su núcleo. Número total de protones en el núcleo se llama el número atómico del átomo y se le da el símbolo Z . La carga eléctrica total del núcleo es, por tanto, + Ze, donde e (carga elemental) es igual a 1,602 x 10-19 culombios .
El carbono es un elemento químico con número atómico 6, lo que significa que hay 6 protones en su núcleo. Número total de protones en el núcleo se llama el número atómico del átomo y se le da el símbolo Z . La carga eléctrica total del núcleo es, por tanto, + Ze, donde e (carga elemental) es igual a 1,602 x 10-19 culombios .
El número total de neutrones en el núcleo de un átomo se llama el número de neutrones del átomo y se le da el símbolo N . Número de neutrones más el número atómico es igual al número de masa atómica: N + Z = A . La diferencia entre el número de neutrones y el número atómico se conoce como exceso de neutrones : D = N – Z = A – 2Z.
Para los elementos estables, suele haber una variedad de isótopos estables. Los isótopos son nucleidos que tienen el mismo número atómico y, por lo tanto, son el mismo elemento, pero difieren en el número de neutrones. Los números de masa de isótopos típicos de carbono son 12; 13.
Principales isótopos de Carbono
El carbono tiene 15 isótopos conocidos, de 8C a 22C, de los cuales 12C y 13C son estables. El radioisótopo de vida más larga es el 14C, con una vida media de 5,730 años.
El carbono-12 es el más abundante de los dos isótopos estables del carbono (siendo el carbono-13 el otro), que asciende al 98,93% del elemento carbono. El carbono-12 es de particular importancia en su uso como el estándar a partir del cual se miden las masas atómicas de todos los nucleidos, por lo tanto, su masa atómica es exactamente 12 daltons por definición. El carbono-12 está compuesto por 6 protones, 6 neutrones y 6 electrones.
El carbono 13 es un isótopo natural y estable de carbono con un núcleo que contiene seis protones y siete neutrones. Como uno de los isótopos ambientales, constituye aproximadamente el 1,1% de todo el carbono natural de la Tierra.
El único radionúclido cosmogénico que contribuye de manera significativa a la exposición interna de los seres humanos es el carbono 14. El carbono 14 radiactivo tiene una vida media de 5730 años y sufre desintegración β− , donde el neutrón se convierte en un protón , un electrón y un antineutrino electrónico. El carbono 14 también se puede producir en la atmósfera mediante otras reacciones de neutrones, que incluyen en particular 13C (n, γ) 14C y 17O(n, α) 14C. Como resultado, el carbono 14 se forma continuamente en la atmósfera superior por la interacción de los rayos cósmicos con el nitrógeno atmosférico. En promedio, solo uno de cada 1,3×1012 átomos de carbono en la atmósfera es un átomo de carbono-14 radiactivo. Como resultado, todas las sustancias biológicas vivas contienen la misma cantidad de C-14 por gramo de carbono, es decir, 0,3 Bq de actividad de carbono 14 por gramo de carbono.
Isótopos estables
| Isótopo | Abundancia | Número de neutrones |
| 12C | 98,9% | 6 |
| 13C | 1,1% | 7 |
Isótopos inestables típicos
| Isótopo | Media vida | Modo de decaimiento | Producto |
| 11C | 20 min | decaimiento beta positivo | 11B |
| 14C | 5730 a | desintegración beta | 14N |
Electrones y configuración electrónica
El número de electrones en un átomo eléctricamente neutro es el mismo que el número de protones en el núcleo. Por lo tanto, el número de electrones en el átomo neutro de Carbono es 6. Cada electrón está influenciado por los campos eléctricos producidos por la carga nuclear positiva y los otros electrones negativos (Z – 1) en el átomo.
Dado que el número de electrones y su disposición son responsables del comportamiento químico de los átomos, el número atómico identifica los diversos elementos químicos. La configuración de estos electrones se deriva de los principios de la mecánica cuántica. El número de electrones en las capas de electrones de cada elemento, particularmente la capa de valencia más externa, es el factor principal para determinar su comportamiento de enlace químico. En la tabla periódica, los elementos se enumeran en orden de número atómico creciente Z.
La configuración electrónica del carbono es [He] 2s2 2p2 .
Los posibles estados de oxidación son -4; -3 …; + 4 .
Se sabe que el carbono forma casi diez millones de compuestos, una gran mayoría de todos los compuestos químicos. Es un elemento tetravalente típico, que hace que cuatro electrones estén disponibles para formar enlaces químicos covalentes. El carbono se encuentra en toda la vida orgánica conocida y es la base de la química orgánica. Cuando se une con el hidrógeno, forma varios hidrocarburos que son importantes para la industria como refrigerantes, lubricantes, solventes, como materia prima química para la fabricación de plásticos y petroquímicos, y como combustibles fósiles.
Compuesto químico de Carbono más común
Las moléculas de dióxido de carbono consisten en un átomo de carbono con doble enlace covalente a dos átomos de oxígeno. El dióxido de carbono es un gas incoloro con una densidad aproximadamente un 53% más alta que la del aire seco. Es relativamente no tóxico y no combustible, pero es más pesado que el aire y puede asfixiarse por el desplazamiento del aire. Cuando el CO2 se disuelve en agua, se forma el ácido carbónico suave. El CO2 enfriado en forma sólida se llama hielo seco. El dióxido de carbono es un componente menor de la atmósfera terrestre, pero un componente importante del aire. Es una materia prima necesaria para la mayoría de las plantas, que eliminan el dióxido de carbono del aire mediante el proceso de fotosíntesis. Una concentración típica de CO2 en el aire es actualmente de aproximadamente 0,040% o 404 ppm. La concentración de dióxido de carbono atmosférico aumenta y disminuye en un patrón estacional en un rango de aproximadamente 6 ppmv. La concentración de CO2 en el aire también ha aumentado constantemente de año en año durante más de 70 años. La tasa actual de aumento es de aproximadamente 2,5 ppm por año.
Resumen
| Elemento | Carbón |
| Numero de protones | 6 |
| Número de neutrones (isótopos típicos) | 12; 13 |
| Numero de electrones | 6 |
| Configuración electronica | [Él] 2s2 2p2 |
| Estados de oxidación | -4; -3 …; + 4 |
Fuente: www.luciteria.com