El oro es un metal brillante, de color amarillo ligeramente rojizo, denso, blando, maleable y dúctil. El oro es un metal de transición y un elemento del grupo 11. Es uno de los elementos químicos menos reactivos y es sólido en condiciones estándar. Se cree que el oro se produjo en la nucleosíntesis de supernovas, a partir de la colisión de estrellas de neutrones.
Protones y neutrones en Oro
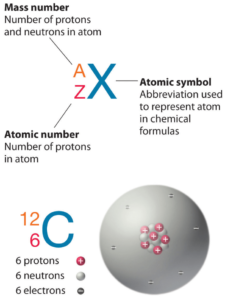 El oro es un elemento químico con número atómico 79, lo que significa que hay 79 protones en su núcleo. Número total de protones en el núcleo se llama el número atómico del átomo y se le da el símbolo Z . La carga eléctrica total del núcleo es, por tanto, + Ze, donde e (carga elemental) es igual a 1,602 x 10-19 culombios .
El oro es un elemento químico con número atómico 79, lo que significa que hay 79 protones en su núcleo. Número total de protones en el núcleo se llama el número atómico del átomo y se le da el símbolo Z . La carga eléctrica total del núcleo es, por tanto, + Ze, donde e (carga elemental) es igual a 1,602 x 10-19 culombios .
El número total de neutrones en el núcleo de un átomo se llama el número de neutrones del átomo y se le da el símbolo N . Número de neutrones más el número atómico es igual al número de masa atómica: N + Z = A . La diferencia entre el número de neutrones y el número atómico se conoce como exceso de neutrones : D = N – Z = A – 2Z.
Para los elementos estables, suele haber una variedad de isótopos estables. Los isótopos son nucleidos que tienen el mismo número atómico y, por lo tanto, son el mismo elemento, pero difieren en el número de neutrones. Los números de masa de isótopos típicos de oro son 197.
Principales isótopos de Oro
El oro se encuentra solo en un isótopo natural: 197Au.
El oro-197 está compuesto por 79 protones, 118 neutrones y 79 electrones.
Isótopos que ocurren naturalmente
| Isótopo | Abundancia | Número de neutrones |
| 197Au | 100% | 118 |
Isótopos inestables típicos
| Isótopo | Media vida | Modo de decaimiento | Producto |
| 195Au | 186,1 d | captura de electrones | 195Pt |
| 196Au | 6,18 d | captura de electrones y desintegración beta | 196Pt y 196Hg |
| 198Au | 2,69 d | desintegración beta | 198Hg |
| 199Au | 3,17 d | desintegración beta | 199Hg |
Electrones y configuración electrónica
El número de electrones en un átomo eléctricamente neutro es el mismo que el número de protones en el núcleo. Por lo tanto, el número de electrones en el átomo neutro de oro es 79. Cada electrón está influenciado por los campos eléctricos producidos por la carga nuclear positiva y los otros electrones negativos (Z – 1) en el átomo.
Dado que el número de electrones y su disposición son responsables del comportamiento químico de los átomos, el número atómico identifica los diversos elementos químicos. La configuración de estos electrones se deriva de los principios de la mecánica cuántica. El número de electrones en las capas de electrones de cada elemento, particularmente la capa de valencia más externa, es el factor principal para determinar su comportamiento de enlace químico. En la tabla periódica, los elementos se enumeran en orden de número atómico creciente Z.
La configuración electrónica del oro es [Xe] 4f14 5d10 6s1 .
Los posibles estados de oxidación son +1,3 .
Aleaciones de Oro más comunes
- Oro amarillo de 18 quilates: 75% oro, 12,5% cobre, 12,5% plata
- Oro amarillo de 18 quilates (más oscuro): 75% oro, 15% cobre, 10% plata
- Oro blanco de 18 quilates: 75% oro, 25% paladio o platino
- Oro blanco de 18 quilates: 75% oro, 10% paladio, 10% níquel y 5% zinc
- Oro rojo de 18 quilates: 75% oro, 25% cobre
- Oro rosa de 18 quilates: 75% oro, 22,25% cobre, 2,75% plata
- Oro rosa de 18 quilates: 75% oro, 20% cobre, 5% plata
- Oro rojo de 12 quilates: 50% oro y 50% cobre
Resumen
| Elemento | Oro |
| Numero de protones | 79 |
| Número de neutrones (isótopos típicos) | 197 |
| Numero de electrones | 79 |
| Configuración electronica | [Xe] 4f14 5d10 6s1 |
| Estados de oxidación | +1,3 |
Fuente: www.luciteria.com