O Ouro é um metal amarelo brilhante, ligeiramente avermelhado, denso, macio, maleável e dúctil. O ouro é um metal de transição e um elemento do grupo 11. É um dos elementos químicos menos reativos e é sólido em condições padrão. Acredita-se que o ouro tenha sido produzido na nucleossíntese de supernova, a partir da colisão de estrelas de nêutrons.
Prótons e nêutrons em Ouro
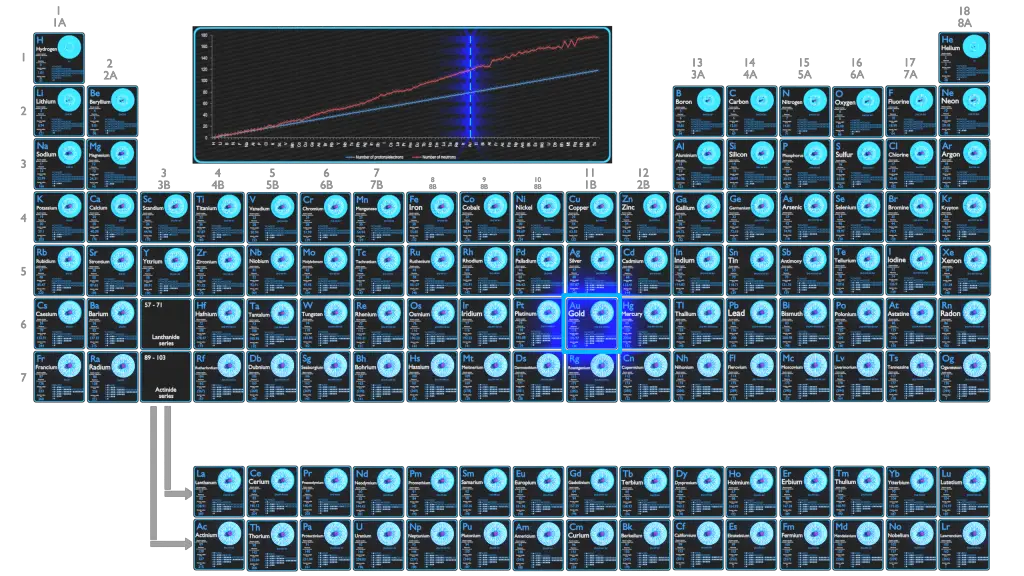
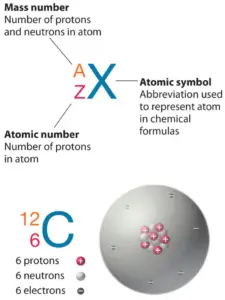 O Ouro é um elemento químico com número atômico 79, o que significa que existem 79 prótons em seu núcleo. O número total de prótons no núcleo é chamado de número atômico do átomo e recebe o símbolo Z. A carga elétrica total do núcleo é, portanto, +Ze, onde e (carga elementar) é igual a 1,602 x 10-19 coulombs.
O Ouro é um elemento químico com número atômico 79, o que significa que existem 79 prótons em seu núcleo. O número total de prótons no núcleo é chamado de número atômico do átomo e recebe o símbolo Z. A carga elétrica total do núcleo é, portanto, +Ze, onde e (carga elementar) é igual a 1,602 x 10-19 coulombs.
O número total de nêutrons no núcleo de um átomo é chamado de número de nêutrons do átomo e recebe o símbolo N. O número de nêutrons mais o número atômico é igual ao número de massa atômica: N+Z=A. A diferença entre o número de nêutrons e o número atômico é conhecida como excesso de nêutrons: D = N – Z = A – 2Z.
Para elementos estáveis, geralmente há uma variedade de isótopos estáveis. Isótopos são nuclídeos que possuem o mesmo número atômico e, portanto, são o mesmo elemento, mas diferem no número de nêutrons. Números de massa de isótopos típicos de Ouro são 197.
Principais isótopos de Ouro
O Ouro ocorre apenas em um isótopo natural – 197Au.
O Ouro-197 é composto de 79 prótons, 118 nêutrons e 79 elétrons.
Isótopos de ocorrência natural
Isótopos Instáveis Típicos
Elétrons e configuração eletrônica
O número de elétrons em um átomo eletricamente neutro é o mesmo que o número de prótons no núcleo. Portanto, o número de elétrons no átomo neutro do Ouro é 79. Cada elétron é influenciado pelos campos elétricos produzidos pela carga nuclear positiva e os outros (Z – 1) elétrons negativos no átomo.
Como o número de elétrons e seu arranjo são responsáveis pelo comportamento químico dos átomos, o número atômico identifica os vários elementos químicos. A configuração desses elétrons segue os princípios da mecânica quântica. O número de elétrons nas camadas de elétrons de cada elemento, particularmente na camada de valência mais externa, é o fator primário na determinação de seu comportamento de ligação química. Na tabela periódica, os elementos são listados em ordem crescente de número atômico Z.
A configuração eletrônica do Ouro é [Xe] 4f14 5d10 6s1.
Possíveis estados de oxidação são +1,3.
Ligas de ouro mais comuns
- Ouro amarelo 18K: 75% ouro, 12,5% cobre, 12,5% prata
- Ouro amarelo 18K (mais escuro): 75% ouro, 15% cobre, 10% prata
- Ouro branco 18K: 75% ouro, 25% de paládio ou platina
- Ouro branco 18K: 75% ouro, 10% paládio, 10% níquel e 5% zinco
- Ouro vermelho 18K: 75% ouro, 25% cobre
- Ouro rosa 18K: 75% ouro, 22,25% cobre, 2,75% prata
- Ouro rosa 18K: 75% ouro, 20% cobre, 5% prata
- Ouro vermelho 12K: 50% ouro e 50% cobre
Sobre os prótons
 Um próton é uma das partículas subatômicas que compõem a matéria. No universo, os prótons são abundantes, constituindo cerca de metade de toda a matéria visível. Tem uma carga elétrica positiva (+1e) e uma massa de repouso igual a 1,67262 × 10−27 kg (938,272 MeV/c2) — ligeiramente mais leve que a do nêutron, mas quase 1,836 vezes maior que a do elétron. O próton tem um raio quadrado médio de cerca de 0,87 × 10−15 m, ou 0,87 fm, e é um spin – ½ férmion.
Um próton é uma das partículas subatômicas que compõem a matéria. No universo, os prótons são abundantes, constituindo cerca de metade de toda a matéria visível. Tem uma carga elétrica positiva (+1e) e uma massa de repouso igual a 1,67262 × 10−27 kg (938,272 MeV/c2) — ligeiramente mais leve que a do nêutron, mas quase 1,836 vezes maior que a do elétron. O próton tem um raio quadrado médio de cerca de 0,87 × 10−15 m, ou 0,87 fm, e é um spin – ½ férmion.
Os prótons existem nos núcleos de átomos típicos, junto com suas contrapartes neutras, os nêutrons. Nêutrons e prótons, comumente chamados de núcleons, estão unidos no núcleo atômico, onde representam 99,9% da massa do átomo. A pesquisa em física de partículas de alta energia no século 20 revelou que nem o nêutron nem o próton não são o menor bloco de construção da matéria.
Sobre Neutrons
Um nêutron é uma das partículas subatômicas que compõem a matéria. No universo, os nêutrons são abundantes, constituindo mais da metade de toda a matéria visível. Ele não tem carga elétrica e uma massa de repouso igual a 1,67493 × 10−27 kg – ligeiramente maior que a do próton, mas quase 1,839 vezes maior que a do elétron. O nêutron tem um raio quadrado médio de cerca de 0,8 × 10−15 m, ou 0,8 fm, e é um férmion spin-½.
Os núcleos atômicos consistem em prótons e nêutrons, que se atraem através da força nuclear, enquanto os prótons se repelem através da força elétrica devido à sua carga positiva. Essas duas forças competem, levando a várias estabilidades de núcleos. Existem apenas certas combinações de nêutrons e prótons, que formam núcleos estáveis.
Os nêutrons estabilizam o núcleo, pois atraem uns aos outros e os prótons, o que ajuda a compensar a repulsão elétrica entre os prótons. Como resultado, à medida que o número de prótons aumenta, uma proporção crescente de nêutrons para prótons é necessária para formar um núcleo estável. Se houver muitos ou poucos nêutrons para um determinado número de prótons, o núcleo resultante não é estável e sofre decaimento radioativo. Isótopos instáveis decaem através de vários caminhos de decaimento radioativo, mais comumente decaimento alfa, decaimento beta ou captura de elétrons. Muitos outros tipos raros de decaimento, como fissão espontânea ou emissão de nêutrons, são conhecidos. Deve-se notar que todas essas vias de decaimento podem ser acompanhadas pela subsequente emissão de radiação gama. Decaimentos alfa ou beta puros são muito raros.
Sobre elétrons e configuração de elétrons
A tabela periódica é uma exibição tabular dos elementos químicos organizados com base em seus números atômicos, configurações eletrônicas e propriedades químicas. A configuração eletrônica é a distribuição de elétrons de um átomo ou molécula (ou outra estrutura física) em orbitais atômicos ou moleculares. O conhecimento da configuração eletrônica de diferentes átomos é útil para entender a estrutura da tabela periódica dos elementos.
Todo sólido, líquido, gás e plasma é composto de átomos neutros ou ionizados. As propriedades químicas do átomo são determinadas pelo número de prótons, na verdade, pelo número e disposição dos elétrons. A configuração desses elétrons segue os princípios da mecânica quântica. O número de elétrons nas camadas de elétrons de cada elemento, particularmente na camada de valência mais externa, é o fator primário na determinação de seu comportamento de ligação química. Na tabela periódica, os elementos são listados em ordem crescente de número atômico Z.
É o princípio de exclusão de Pauli que exige que os elétrons de um átomo ocupem diferentes níveis de energia, em vez de todos se condensarem no estado fundamental. A ordenação dos elétrons no estado fundamental de átomos multieletrônicos começa com o estado de energia mais baixo (estado fundamental) e se move progressivamente a partir daí na escala de energia até que cada um dos elétrons do átomo receba um conjunto único de números quânticos. Este fato tem implicações importantes para a construção da tabela periódica dos elementos.
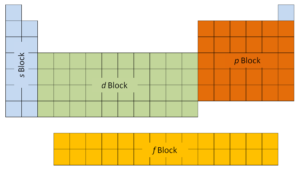 As duas primeiras colunas do lado esquerdo da tabela periódica são onde os subníveis s estão sendo ocupados. Por causa disso, as duas primeiras linhas da tabela periódica são rotuladas como o bloco s. Da mesma forma, o bloco p são as seis colunas mais à direita da tabela periódica, o bloco d são as 10 colunas intermediárias da tabela periódica, enquanto o bloco f é a seção de 14 colunas que normalmente é descrita como separada do corpo principal da tabela periódica. Poderia ser parte do corpo principal, mas então a tabela periódica seria bastante longa e complicada.
As duas primeiras colunas do lado esquerdo da tabela periódica são onde os subníveis s estão sendo ocupados. Por causa disso, as duas primeiras linhas da tabela periódica são rotuladas como o bloco s. Da mesma forma, o bloco p são as seis colunas mais à direita da tabela periódica, o bloco d são as 10 colunas intermediárias da tabela periódica, enquanto o bloco f é a seção de 14 colunas que normalmente é descrita como separada do corpo principal da tabela periódica. Poderia ser parte do corpo principal, mas então a tabela periódica seria bastante longa e complicada.
Para átomos com muitos elétrons, essa notação pode se tornar extensa e, portanto, uma notação abreviada é usada. A configuração eletrônica pode ser visualizada como os elétrons do núcleo, equivalentes ao gás nobre do período anterior, e os elétrons de valência (por exemplo, [Xe] 6s2 para o bário).
Estados de Oxidação
Os estados de oxidação são tipicamente representados por números inteiros que podem ser positivos, zero ou negativos. A maioria dos elementos tem mais de um estado de oxidação possível. Por exemplo, o carbono tem nove possíveis estados inteiros de oxidação de -4 a +4.
A definição atual do IUPAC Gold Book de estado de oxidação é:
“O estado de oxidação de um átomo é a carga desse átomo após a aproximação iônica de suas ligações heteronucleares…”
e o termo número de oxidação é quase sinônimo. Um elemento que não é combinado com nenhum outro elemento diferente tem um estado de oxidação de 0. O estado de oxidação 0 ocorre para todos os elementos – é simplesmente o elemento em sua forma elementar. Um átomo de um elemento em um composto terá um estado de oxidação positivo se tiver seus elétrons removidos. Da mesma forma, a adição de elétrons resulta em um estado de oxidação negativo. Também distinguimos entre os estados de oxidação possíveis e comuns de cada elemento. Por exemplo, o silício tem nove possíveis estados inteiros de oxidação de -4 a +4, mas apenas -4, 0 e +4 são estados de oxidação comuns.
Resumo
| Elemento |
Ouro |
| Número de prótons |
79 |
| Número de nêutrons (isótopos típicos) |
197 |
| Número de elétrons |
79 |
| configuração eletrônica |
[Veículo] 4f14 5d10 6s1 |
| Estados de oxidação |
+1,3 |

Fonte: www.luciteria.com
Propriedades de outros elementos
Outras propriedades do Ouro
 O Ouro é um elemento químico com número atômico 79, o que significa que existem 79 prótons em seu núcleo. O número total de prótons no núcleo é chamado de número atômico do átomo e recebe o símbolo Z. A carga elétrica total do núcleo é, portanto, +Ze, onde e (carga elementar) é igual a 1,602 x 10-19 coulombs.
O Ouro é um elemento químico com número atômico 79, o que significa que existem 79 prótons em seu núcleo. O número total de prótons no núcleo é chamado de número atômico do átomo e recebe o símbolo Z. A carga elétrica total do núcleo é, portanto, +Ze, onde e (carga elementar) é igual a 1,602 x 10-19 coulombs.