Le rhodium est un métal de transition rare, blanc argenté, dur, résistant à la corrosion et chimiquement inerte. C’est un métal noble et un membre du groupe du platine.
Protons et neutrons dans le Rhodium
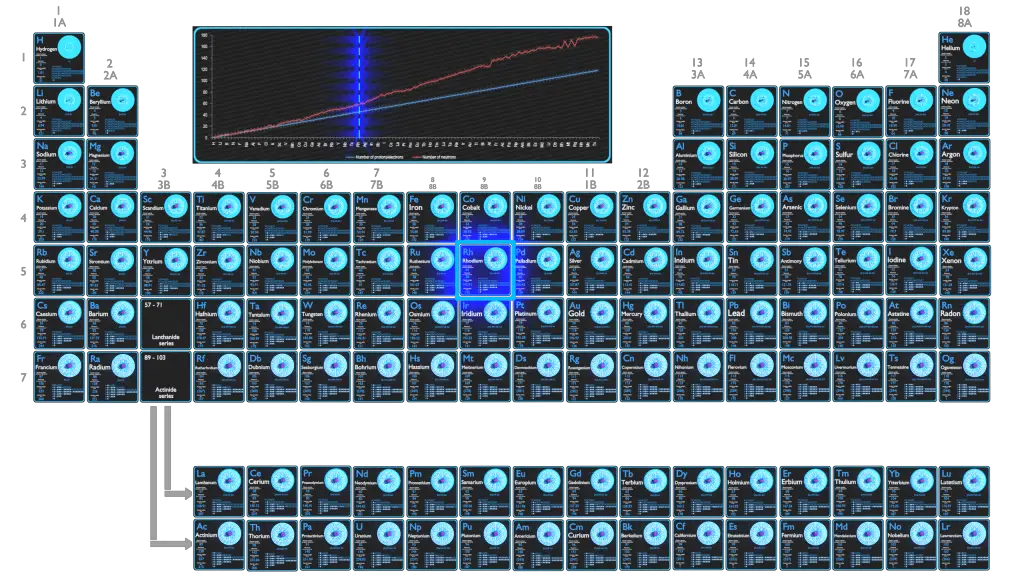
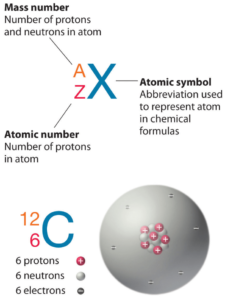 Le rhodium est un élément chimique de numéro atomique 45, ce qui signifie qu’il y a 45 protons dans son noyau. Le nombre total de protons dans le noyau est appelé le numéro atomique de l’atome et reçoit le symbole Z. La charge électrique totale du noyau est donc +Ze, où e (charge élémentaire) vaut 1 602 x 10-19 coulombs.
Le rhodium est un élément chimique de numéro atomique 45, ce qui signifie qu’il y a 45 protons dans son noyau. Le nombre total de protons dans le noyau est appelé le numéro atomique de l’atome et reçoit le symbole Z. La charge électrique totale du noyau est donc +Ze, où e (charge élémentaire) vaut 1 602 x 10-19 coulombs.
Le nombre total de neutrons dans le noyau d’un atome est appelé le nombre de neutrons de l’atome et reçoit le symbole N. Le nombre de neutrons plus le numéro atomique est égal au nombre de masse atomique: N+Z=A. La différence entre le nombre de neutrons et le numéro atomique est appelée excès de neutrons: D = N – Z = A – 2Z.
Pour les éléments stables, il existe généralement une variété d’isotopes stables. Les isotopes sont des nucléides qui ont le même numéro atomique et sont donc le même élément, mais diffèrent par le nombre de neutrons. Les nombres de masse des isotopes typiques du rhodium sont de 103.
Principaux isotopes du Rhodium
Le rhodium n’est présent que dans un seul isotope naturel – 103Rh.
Le rhodium-103 est composé de 45 protons, 58 neutrons et 45 électrons.
Isotopes instables typiques
| Isotope | Demi-vie | Mode de décomposition | Produit |
| 99Rh | 16,1 j | capture d’électrons | 99Ru |
| 101mRh | 4,34 j | capture d’électrons ou IT | 101Ru ou101Rh |
| 101Rh | 3,3 a | capture d’électrons | 101Ru |
| 102mRh | 3,7 a | capture d’électrons | 102Ru |
| 102Rh | 207 j | désintégration bêta | 102Pd |
| 105Rh | 35 h 36 | désintégration bêta | 105Pd |
Électrons et configuration électronique
Le nombre d’électrons dans un atome électriquement neutre est le même que le nombre de protons dans le noyau. Par conséquent, le nombre d’électrons dans l’atome neutre de Rhodium est de 45. Chaque électron est influencé par les champs électriques produits par la charge nucléaire positive et les autres (Z – 1) électrons négatifs dans l’atome.
Le nombre d’électrons et leur disposition étant responsables du comportement chimique des atomes, le numéro atomique identifie les différents éléments chimiques. La configuration de ces électrons découle des principes de la mécanique quantique. Le nombre d’électrons dans les couches d’électrons de chaque élément, en particulier la couche de valence la plus externe, est le principal facteur déterminant son comportement de liaison chimique. Dans le tableau périodique, les éléments sont classés par ordre croissant de numéro atomique Z.
La configuration électronique du rhodium est [Kr] 4d8 5s1.
Les états d’oxydation possibles sont +3.
Application la plus courante du Rhodium
L’utilisation principale de l’élément (environ 80 % de la production mondiale de rhodium) est l’un des catalyseurs des convertisseurs catalytiques à trois voies dans les automobiles. Les convertisseurs catalytiques à trois voies ont l’avantage supplémentaire de contrôler les émissions d’oxyde nitrique (NO) et d’azote. dioxyde.
Résumé
| Élément | Rhodium |
| Nombre de protons | 45 |
| Nombre de neutrons (isotopes typiques) | 103 |
| Nombre d’électrons | 45 |
| Configuration électronique | [Kr] 4d8 5s1 |
| États d’oxydation | +3 |
Source : www.luciteria.com