O Radônio é um gás nobre radioativo, incolor, inodoro e insípido. O radônio ocorre naturalmente como um passo intermediário nas cadeias normais de decaimento radioativo através das quais o tório e o urânio decaem lentamente em chumbo.
Prótons e nêutrons no Radônio
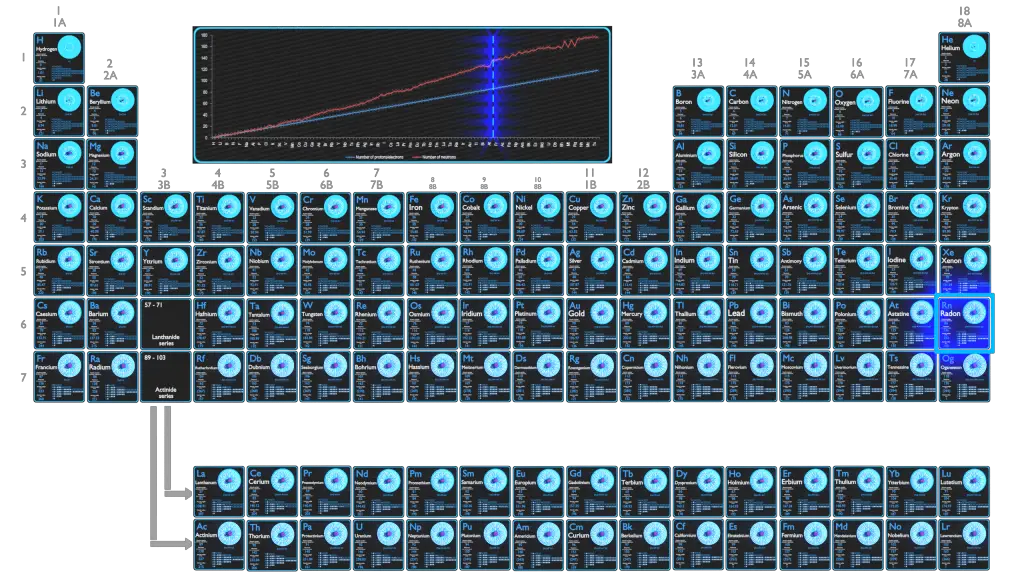
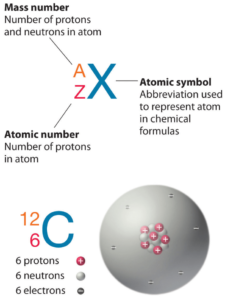 O Radônio é um elemento químico com número atômico 86, o que significa que existem 86 prótons em seu núcleo. O número total de prótons no núcleo é chamado de número atômico do átomo e recebe o símbolo Z. A carga elétrica total do núcleo é, portanto, +Ze, onde e (carga elementar) é igual a 1,602 x 10-19 coulombs.
O Radônio é um elemento químico com número atômico 86, o que significa que existem 86 prótons em seu núcleo. O número total de prótons no núcleo é chamado de número atômico do átomo e recebe o símbolo Z. A carga elétrica total do núcleo é, portanto, +Ze, onde e (carga elementar) é igual a 1,602 x 10-19 coulombs.
O número total de nêutrons no núcleo de um átomo é chamado de número de nêutrons do átomo e recebe o símbolo N. O número de nêutrons mais o número atômico é igual ao número de massa atômica: N+Z=A . A diferença entre o número de nêutrons e o número atômico é conhecida como excesso de nêutrons: D = N – Z = A – 2Z.
Para elementos estáveis, geralmente há uma variedade de isótopos estáveis. Isótopos são nuclídeos que possuem o mesmo número atômico e, portanto, são o mesmo elemento, mas diferem no número de nêutrons. Números de massa de isótopos típicos de Radônio são 222.
Principais isótopos do Radônio
O Radônio ocorre na forma natural – apenas nos isótopos 222Rn. O 222Rn ocorre apenas em traços e é levemente radioativo, decaindo por decaimento alfa com uma meia-vida de 3,8235 dias.
Radon-222 é composto de 86 prótons, 136 nêutrons e 86 elétrons.
Isótopos de ocorrência natural
| Isótopo | Abundância | número de nêutrons |
| 222Rn (instável) | vestígio | 136 |
Isótopos Instáveis Típicos
| Isótopo | Meia-vida | Modo Decaimento | produtos |
| 210Rn | 6×104 a | decaimento alfa | 206Po |
| 211Rn | 14,6 h | captura de elétrons ou decaimento alfa | 211At ou 207Po |
| 222Rn | 3,8235 d | decaimento alfa | 218Po |
| 224Rn | 2,4 h | decaimento beta | 224Fr |
Elétrons e configuração eletrônica
O número de elétrons em um átomo eletricamente neutro é o mesmo que o número de prótons no núcleo. Portanto, o número de elétrons no átomo neutro de Radônio é 86. Cada elétron é influenciado pelos campos elétricos produzidos pela carga nuclear positiva e os outros (Z – 1) elétrons negativos no átomo.
Como o número de elétrons e seu arranjo são responsáveis pelo comportamento químico dos átomos, o número atômico identifica os vários elementos químicos. A configuração desses elétrons segue os princípios da mecânica quântica. O número de elétrons nas camadas de elétrons de cada elemento, particularmente na camada de valência mais externa, é o fator primário na determinação de seu comportamento de ligação química. Na tabela periódica, os elementos são listados em ordem crescente de número atômico Z.
A configuração eletrônica do Radônio é [Hg] 6p6.
Os possíveis estados de oxidação são 0.
Resumo
| Elemento | Radônio |
| Número de prótons | 86 |
| Número de nêutrons (isótopos típicos) | 222 |
| Número de elétrons | 86 |
| configuração eletrônica | [Hg] 6p6 |
| Estados de oxidação | 0 |
Fonte: www.luciteria.com