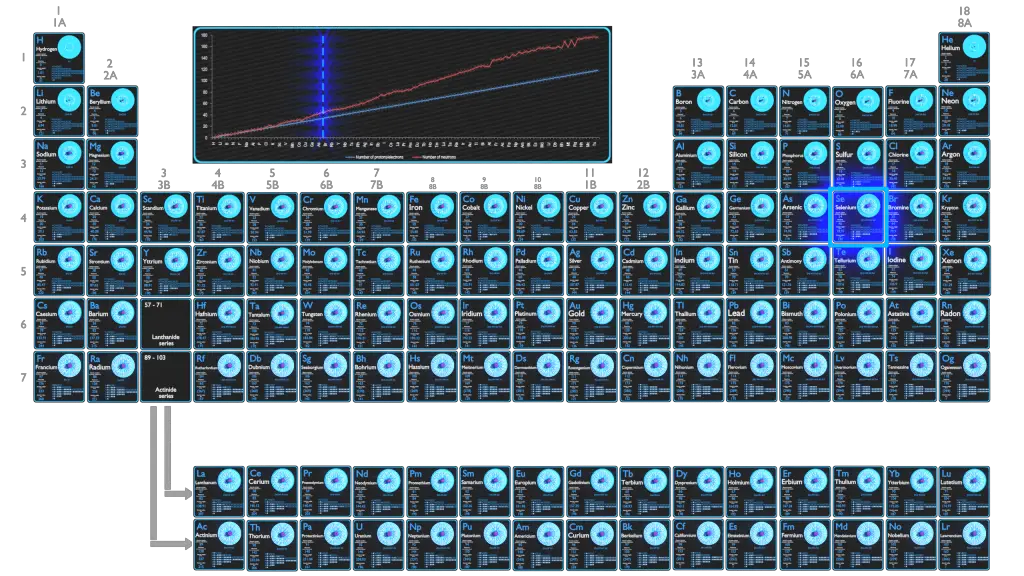
O Selênio é um não-metal com propriedades intermediárias entre os elementos acima e abaixo na tabela periódica, enxofre e telúrio, e também possui semelhanças com o arsênico. Raramente ocorre em seu estado elementar ou como compostos de minério puro na crosta terrestre.
Prótons e nêutrons no Selênio
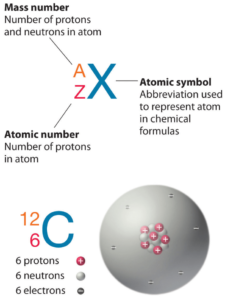 O Selênio é um elemento químico com número atômico 34, o que significa que existem 34 prótons em seu núcleo. O número total de prótons no núcleo é chamado de número atômico do átomo e recebe o símbolo Z. A carga elétrica total do núcleo é, portanto, +Ze, onde e (carga elementar) é igual a 1,602 x 10-19 coulombs.
O Selênio é um elemento químico com número atômico 34, o que significa que existem 34 prótons em seu núcleo. O número total de prótons no núcleo é chamado de número atômico do átomo e recebe o símbolo Z. A carga elétrica total do núcleo é, portanto, +Ze, onde e (carga elementar) é igual a 1,602 x 10-19 coulombs.
O número total de nêutrons no núcleo de um átomo é chamado de número de nêutrons do átomo e recebe o símbolo N. O número de nêutrons mais o número atômico é igual ao número de massa atômica: N+Z=A. A diferença entre o número de nêutrons e o número atômico é conhecida como excesso de nêutrons: D = N – Z = A – 2Z.
Para elementos estáveis, geralmente há uma variedade de isótopos estáveis. Isótopos são nuclídeos que possuem o mesmo número atômico e, portanto, são o mesmo elemento, mas diferem no número de nêutrons. Números de massa de isótopos típicos de Selênio são 74; 76; 77; 78; 80.
Principais isótopos do Selênio
O Selênio ocorre em 5 isótopos naturais: 74Se, 76Se, 77Se, 78Se, 79Se, 80Se e 82Se. Destes, 79Se é um radioisótopo traço, decaindo por decaimento beta com uma meia-vida de 3,27×105 anos. 82Se está decaindo por decaimento beta duplo com uma meia-vida de 1,08 × 1020 anos. O 80Se é o isótopo mais comum, tendo uma abundância natural de aproximadamente 49,8%.
O Selênio-74 é composto de 34 prótons, 40 nêutrons e 34 elétrons.
O Selênio-76 é composto por 34 prótons, 42 nêutrons e 34 elétrons.
O Selênio-77 é composto de 34 prótons, 43 nêutrons e 34 elétrons.
O Selênio-78 é composto de 34 prótons, 44 nêutrons e 34 elétrons.
O Selênio-79 é composto por 34 prótons, 45 nêutrons e 34 elétrons.
O Selênio-80 é composto de 34 prótons, 46 nêutrons e 34 elétrons.
O Selênio-82 é composto de 34 prótons, 48 nêutrons e 34 elétrons.
Isótopos de ocorrência natural
| Isótopo | Abundância | número de nêutrons |
| 74Se | 0,86% | 40 |
| 76Se | 9,23% | 42 |
| 77Se | 7,60% | 43 |
| 78Se | 23,69% | 44 |
| 79Se | vestígio | 45 |
| 80Se | 49,80% | 46 |
| 82Se (instável) | 8,82% | 48 |
Isótopos Instáveis Típicos
| Isótopo | Meia-vida | Modo Decaimento | produtos |
| 72Se | 8,4 d | captura eletrônica | 72As |
| 75Se | 119,8 d | captura eletrônica | 75As |
| 79Se | 3,27×105 a | decaimento beta | 79Br |
| 82Se | 1,08×1020 a | decaimento beta | 82Kr |
Elétrons e configuração eletrônica
O número de elétrons em um átomo eletricamente neutro é o mesmo que o número de prótons no núcleo. Portanto, o número de elétrons no átomo neutro do Selênio é 34. Cada elétron é influenciado pelos campos elétricos produzidos pela carga nuclear positiva e os outros (Z – 1) elétrons negativos no átomo.
Como o número de elétrons e seu arranjo são responsáveis pelo comportamento químico dos átomos, o número atômico identifica os vários elementos químicos. A configuração desses elétrons segue os princípios da mecânica quântica. O número de elétrons nas camadas de elétrons de cada elemento, particularmente na camada de valência mais externa, é o fator primário na determinação de seu comportamento de ligação química. Na tabela periódica, os elementos são listados em ordem crescente de número atômico Z.
A configuração eletrônica do Selênio é [Ar] 3d10 4s2 4p4.
Possíveis estados de oxidação são +4,6/-2.
Aplicação mais comum de Selênio
Os principais usos comerciais do selênio atualmente são a fabricação de vidro e os pigmentos. O selênio encontra aplicações em diversas indústrias, por exemplo, células solares e aplicações fotocondutoras.
A tabela periódica é uma exibição tabular dos elementos químicos organizados com base em seus números atômicos, configurações eletrônicas e propriedades químicas. A configuração eletrônica é a distribuição de elétrons de um átomo ou molécula (ou outra estrutura física) em orbitais atômicos ou moleculares. O conhecimento da configuração eletrônica de diferentes átomos é útil para entender a estrutura da tabela periódica dos elementos.
Todo sólido, líquido, gás e plasma é composto de átomos neutros ou ionizados. As propriedades químicas do átomo são determinadas pelo número de prótons, na verdade, pelo número e disposição dos elétrons. A configuração desses elétrons segue os princípios da mecânica quântica. O número de elétrons nas camadas de elétrons de cada elemento, particularmente na camada de valência mais externa, é o fator primário na determinação de seu comportamento de ligação química. Na tabela periódica, os elementos são listados em ordem crescente de número atômico Z.
É o princípio de exclusão de Pauli que exige que os elétrons de um átomo ocupem diferentes níveis de energia, em vez de todos se condensarem no estado fundamental. A ordenação dos elétrons no estado fundamental de átomos multieletrônicos começa com o estado de energia mais baixo (estado fundamental) e se move progressivamente a partir daí na escala de energia até que cada um dos elétrons do átomo receba um conjunto único de números quânticos. Este fato tem implicações importantes para a construção da tabela periódica dos elementos.
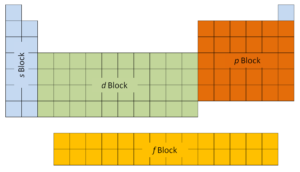 As duas primeiras colunas do lado esquerdo da tabela periódica são onde os subníveis s estão sendo ocupados. Por causa disso, as duas primeiras linhas da tabela periódica são rotuladas como o bloco s. Da mesma forma, o bloco p são as seis colunas mais à direita da tabela periódica, o bloco d são as 10 colunas intermediárias da tabela periódica, enquanto o bloco f é a seção de 14 colunas que normalmente é descrita como separada do corpo principal da tabela periódica. Poderia ser parte do corpo principal, mas então a tabela periódica seria bastante longa e complicada.
As duas primeiras colunas do lado esquerdo da tabela periódica são onde os subníveis s estão sendo ocupados. Por causa disso, as duas primeiras linhas da tabela periódica são rotuladas como o bloco s. Da mesma forma, o bloco p são as seis colunas mais à direita da tabela periódica, o bloco d são as 10 colunas intermediárias da tabela periódica, enquanto o bloco f é a seção de 14 colunas que normalmente é descrita como separada do corpo principal da tabela periódica. Poderia ser parte do corpo principal, mas então a tabela periódica seria bastante longa e complicada.
Para átomos com muitos elétrons, essa notação pode se tornar extensa e, portanto, uma notação abreviada é usada. A configuração eletrônica pode ser visualizada como os elétrons do núcleo, equivalentes ao gás nobre do período anterior, e os elétrons de valência (por exemplo, [Xe] 6s2 para o bário).
Estados de Oxidação
Os estados de oxidação são tipicamente representados por números inteiros que podem ser positivos, zero ou negativos. A maioria dos elementos tem mais de um estado de oxidação possível. Por exemplo, o carbono tem nove possíveis estados inteiros de oxidação de -4 a +4.
A definição atual do IUPAC Gold Book de estado de oxidação é:
"O estado de oxidação de um átomo é a carga desse átomo após a aproximação iônica de suas ligações heteronucleares..."
e o termo número de oxidação é quase sinônimo. Um elemento que não é combinado com nenhum outro elemento diferente tem um estado de oxidação de 0. O estado de oxidação 0 ocorre para todos os elementos – é simplesmente o elemento em sua forma elementar. Um átomo de um elemento em um composto terá um estado de oxidação positivo se tiver seus elétrons removidos. Da mesma forma, a adição de elétrons resulta em um estado de oxidação negativo. Também distinguimos entre os estados de oxidação possíveis e comuns de cada elemento. Por exemplo, o silício tem nove possíveis estados inteiros de oxidação de -4 a +4, mas apenas -4, 0 e +4 são estados de oxidação comuns.
[/with_spoiler]
Resumo
| Elemento | Selênio |
| Número de prótons | 34 |
| Número de nêutrons (isótopos típicos) | 74; 76; 77; 78; 80 |
| Número de elétrons | 34 |
| configuração eletrônica | [Ar] 3d10 4s2 4p4 |
| Estados de oxidação | +4,6/-2 |
Fonte: www.luciteria.com